Redacción Farmacosalud.com
“Los fármacos que inhiben el SGLT-2 son los que buscamos porque son los que van a inhibir la reabsorción tubular de glucosa, provocando glucosuria (pérdida de glucosa por el riñón y disminuyendo los niveles de glucosa). Aquellos que consiguen una pequeña inhibición de los SGLT-1 tienen el valor añadido de conseguir disminución de los niveles de hiperglucemia postpandrial”. Así se expresa el doctor Elías Delgado en una entrevista sobre las combinaciones en el manejo de la diabetes. El doctor también alude a la capacidad de los inhibidores de la SGLT-2 para contribuir a la pérdida de peso: “Al eliminar glucosa por el riñón, son calorías que eliminamos del organismo. A la vez producen un efecto glucosúrico, con lo cual arrastran agua. Se pensaba que podría ser un efecto exclusivamente de volumen de líquido, pero claramente se ha comprobado que las dos terceras partes del peso que se pierde -de media pueden ser unos 4-5 Kilos- son de masa grasa. Está claro: tú pierdes glucosa por el riñón, pierdes calorías y disminuyes peso”. Asimismo, Delgado, que es médico del Servicio de Endocrinología y Nutrición del Hospital Universitario Central de Asturias (Oviedo) y profesor titular de la Facultad de Medicina de Oviedo, recuerda que esta nueva familia de fármacos tiene un efecto “beneficioso no sólo en términos de hiperglucemia y peso, sino también” en términos de hipertensión arterial “porque disminuye la tensión arterial”.

Doctor Elías Delgado
Fuente: Dr. Delgado
-¿El riñón es un actor importante en el ámbito de la regulación del metabolismo de la glucosa?
Sí, el riñón es uno de los órganos que teníamos prácticamente olvidado en la fisiopatología de la diabetes, simplemente se tenía como un actor que sufría los efectos de la hiperglucemia. Pero a medida que se va conociendo mejor la fisiopatología de la enfermedad, se ve que el riñón participa también en el aumento de la concentración de glucosa en el organismo del paciente diabético. Por decirlo de alguna manera muy sencilla, el riñón filtra glucosa y reabsorbe glucosa. Los pacientes diabéticos reabsorben más concentración de glucosa, lo cual perpetúa esa hiperglucemia, que es el problema fundamental que tienen los pacientes con diabetes. Por lo tanto, podríamos decir que el riñón no sólo sufre los efectos de la hiperglucemia, sino que participa de una forma activa en que los niveles de glucosa en los pacientes con diabetes estén más elevados porque tiene una mayor concentración de las proteínas-transportadoras que reabsorben la glucosa.
-¿Qué han representado en el manejo de la diabetes los nuevos inhibidores del cotransportador sodio-glucosa (SGLT)?
Han sido una gran aportación en el arsenal terapéutico de la diabetes porque, por así decirlo, son los primeros fármacos orales que permiten disminuir los niveles de glucosa en el diabético y a la vez disminuir peso y tensión arterial, problemas para los que teníamos muy pocos tratamientos. Hasta hace muy poco todos los fármacos que controlaban los niveles de glucosa tenían el efecto secundario de aumento de peso. Desde hace unos años tenemos fármacos inyectables que también disminuyen el peso. Pero los primeros fármacos de administración oral que hacen las dos cosas -disminuir los niveles de glucosa al tiempo que disminuyen peso y tensión arterial- son los fármacos glucosúricos, los inhibidores del cotransportador sodio-glucosa a nivel del túbulo contorneado proximal. Por lo tanto, es una nueva aportación muy atractiva para una gran parte de nuestra población diabética. Tenemos que recordar que prácticamente el 75-80% de los pacientes con diabetes tipo 2 van a tener obesidad.
-¿Qué diferencia sustancial hay entre SGLT-1 y SGLT-2?
El SGLT es un cotransportador sodio-glucosa, que se encuentra en diversas partes del organismo. La función que tienen esos cotransportadores es, fundamentalmente, reabsorber la glucosa, asociada con una reabsorción de sodio conjunta. Es una familia de cotransportadores de la que se han descubierto numerosos miembros, incluso hasta seis de ellos. La familia del número 2 se sitúa fundamentalmente a nivel del túbulo contorneado proximal y su capacidad básica es la de reabsorber glucosa a nivel del mencionado túbulo, mientras que el SGLT-1 no solamente se dedica a la reabsorción de glucosa, sino también a la de galactosa, y se encuentra principalmente en el intestino delgado, aunque también en un pequeño porcentaje a nivel del riñón.
Luego, hay una serie de familias que tienen menos trascendencia. En resumen, es una misma familia con distintos componentes con un concepto de misión general en el organismo: reabsorber glucosa acoplada a la reabsorción de sodio. El humano ingiere glucosa, el SGLT-1 a nivel intestinal reabsorbe la glucosa y la introduce en el torrente sanguíneo y después el riñón filtra toda esa glucosa por el glomérulo y posteriormente va a ser reabsorbida por el SGLT-2 en un 90%, el 10% restante por vía SGLT-1. En definitiva, son dos miembros de una misma familia, con una misma acción (reabsorber glucosa) pero con distintas ubicaciones: el 2 a nivel renal y el 1 a nivel del intestino delgado.
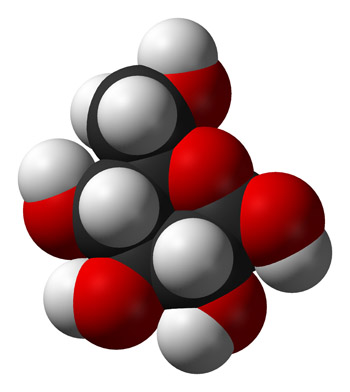
β-D-Glucosa
Dominio Público
Fuente: Viquipèdia / Wikimedia Commons
-¿SGLT-1 y SGLT-2 son una buena combinación en el tratamiento de la diabetes tipo 2?
Lo que nosotros hemos visto es que los inhibidores del SGLT-2 disminuyen el umbral de reabsorción de glucosa, con lo cual el paciente elimina glucosa por el riñón, reduciéndose los niveles de este componente a nivel del torrente sanguíneo. Es decir, disminuye su hiperglucemia. Estábamos acostumbrados a ver como los fármacos con mayor especificidad por su receptor era mejores. Sin embargo, se está viendo que algún fármaco que no es tan selectivo y que tiene una pequeña inhibición a nivel de SGLT-1 puede aportar una ligera ventaja, sobre todo por la disminución de la hiperglucemia postpandrial. Disminuyen los niveles de insulina y de glucosa postpandrial al inhibir ligeramente y transitoriamente los SGLT-1 a nivel intestinal, con lo cual la absorción de glucosa en el intestino no tiene lugar de una forma tan rápida como en un paciente normal. Eso está claro y hay diferencias entre los inhibidores que tienen más o menos selectividad por el receptor de SGLT-2; está claramente demostrado en estudios comparativos a nivel farmacodinámica-farmacocinética en los niveles de glucosa. En los ensayos clínicos también se ve una pequeña mayor potencia en dosis por encima de 200 microgramos, que probablemente es donde está el umbral de una pequeña inhibición del SGLT-1, teniendo mayor transcendencia a nivel de disminución de la hiperglucemia postpandrial.
En resumen, los fármacos que inhiben el SGLT-2 son los que buscamos porque son los que van a inhibir la reabsorción tubular de glucosa, provocando glucosuria (pérdida de glucosa por el riñón y disminuyendo los niveles de glucosa). Aquellos que consiguen una pequeña inhibición de los SGLT-1 tienen el valor añadido de conseguir disminución de los niveles de hiperglucemia postpandrial. De todas maneras, estos son conceptos que están en farmacodinámica-farmacocinética; lo ideal sería disponer de la evidencia, que sería aquel ensayo clínico que compara uno más selectivo contra el SGLT-2 versus aquel que tiene menor especificidad y también inhibe ligeramente los SGLT-1.
-¿Cómo se explica que los nuevos fármacos inhibidores de la SGLT-2 contribuyan además a la pérdida de peso en los pacientes con diabetes tipo 2?
Al eliminar glucosa por el riñón, son calorías que eliminamos del organismo. A la vez producen un efecto glucosúrico, con lo cual arrastran agua. Se pensaba que podría ser un efecto exclusivamente de volumen de líquido, pero claramente se ha comprobado que las dos terceras partes del peso que se pierde -de media pueden ser unos 4-5 Kilos- son de masa grasa. Está claro: tú pierdes glucosa por el riñón, pierdes calorías y disminuyes peso.

Autor/a: Coyau
Fuente: Wikimedia Commons
-¿Por término medio, qué pérdida de peso obtienen, sin hiperglucemia?
La media de los ensayos clínicos nos sitúan en torno a los 3-5 kilos de peso, y la característica fundamental es que parece que esa pérdida de peso se mantiene a lo largo del tiempo. Estamos cansados de ver en los ensayos de medicación antiobesidad que el efecto es muy temporal… hay un rebote y tienden a ir hacia el peso que tenían previamente. Con el grupo de fármacos al que nos referíamos, lo atractivo es que hay una pérdida de peso significativa, alrededor de unos 5 kilos de peso, y lo verdaderamente interesante es que se mantiene a lo largo del tiempo. Algunos de los fármacos tienen ya evidencia de hasta los 4 años de seguimiento.
-Se espera poder contar con otras moléculas del mismo grupo en poco tiempo. ¿Habrá diferencias sustanciales?
Estamos en ensayos clínicos que comparan una contra otra. Está claro que se trata de una familia muy atractiva y las sutilezas entre los distintos miembros de esta familia ya nos va a costar más diferenciarlas; a nivel fármacocinético-farmacodinámico hay claridad y lo que necesitamos son evidencias, como siempre andamos en medicina. Y la evidencia no vamos a tenerla hasta que no haya ese estudio comparando uno contra otro.
-¿Qué podemos decir de la seguridad a medio o largo plazo en esta nueva familia de fármacos?
Tenemos ensayos con un seguimiento de hasta 4-5 años, y parece que la seguridad está garantizada. Está claro que tienen algunos efectos secundarios, fundamentalmente al aumentar la concentración de glucosa de la orina: nos va a aumentar discretamente la incidencia de infecciones urinarias y de infecciones genitales, fundamentalmente en la mujer. Pero será de una manera discreta: en infecciones urinarias un 5-6% y las infecciones genitales pueden rondar el 10-11%. Entonces tendremos que seleccionar a aquellos pacientes que tengan riesgo de infecciones genitales o que hayan tenido historia previa de infecciones urinarias como pacientes que no serán candidatos ideales para esta nueva familia terapéutica. Sin embargo, para la gran mayoría de los pacientes a quienes se administra esta medicación y que tienen ese 10-11% de infecciones genitales, el tratamiento es muy leve y sencillo.
Autor/a: Enric Arandes
Fuente: E. Arandes / www.farmacosalud.com
La otra cara de la moneda en cuanto a seguridad es la seguridad cardiovascular. Porque no perdamos de vista que nosotros tratamos a los diabéticos para prevenir sus problemas cardiovasculares a largo plazo, que es de lo que se nos mueren nuestros diabéticos. Así, no nos basta que bajen los niveles de glucosa, no nos basta que baje el peso, no nos basta que baje la tensión arterial, sino que querríamos demostrar que conseguimos con todo ello una disminución de los eventos cardiovasculares a largo plazo. Hay ensayos clínicos en marcha, pero probablemente hasta 2016 o más tarde no conoceremos sus resultados. Los metaanálisis de los ensayos que se han presentado para la aprobación por parte de las agencias reguladoras son muy tranquilizadores y tienen un efecto neutro sobre la salud cardiovascular. Son fármacos seguros en el ámbito cardiovascular.
-¿Qué más puede añadir sobre el hecho de que la nueva familia de fármacos sea eficaz en diabéticos hipertensos?
Claro, no dejan de ser un antihipertensivo. Al producir glucosuria actúan como un diurético y se elimina glucosa, con lo cual disminuye la tensión en la población general… hasta 5 mmHg de descenso en la tensión arterial sistólica. E incluso en aquellos pacientes hipertensos hay mayores descensos, llegando a los 10-12 milímetros de mercurio. Por lo tanto, el efecto es beneficioso no sólo en términos de hiperglucemia y peso, sino también porque disminuye la tensión arterial. Eso tendremos que tenerlo en cuenta en aquellos pacientes hipertensos que ya estén en tratamiento y a los que probablemente tengamos que reajustar sus dosis y/o asociarles otro antihipertensivo. Por lo tanto, es un tercer valor añadido. Sobre el tema de las hipoglucemias -el otro gran riesgo que teníamos con numerosos medicamentos previos-, los nuevos fármacos no producen hipoglucemia; el riesgo de hipoglucemia que van a tener esos pacientes va a ser muy pequeñito.
-¿Vamos hacia una medicina personalizada también en diabetes?
Sí, de una manera gráfica lo presento de la siguiente manera: los médicos que tratamos diabéticos, igual que en otras patologías, acabamos siendo un poquito magos, porque tenemos que conjugar la evidencia clínica, que no es toda la que nosotros desearíamos, con nuestra experiencia, las necesidades del paciente y las distintas opciones terapéuticas que tenemos. Entonces, hay que individualizar el tratamiento para el enfermo que tenemos delante. Y ojalá podamos ir incorporando a nuestros pacientes un tema muy atractivo que en otros campos de la medicina está teniendo presencia: la farmacogenómica, es decir, las distintas reacciones al tratamiento dependiendo de los genes que uno tenga. Hasta entonces, lo que tendremos que hacer es ser hábiles y captar todas las señales… generalmente, en diabetes vamos a tener que ir siempre a un tratamiento combinado y abordar la enfermedad desde distintos ámbitos, sabiendo que existen diversas alteraciones fisiopatológicas. Hay que abordar esas alteraciones con tratamiento combinado y buscar cuál es la combinación más adecuada para cada uno de los pacientes. De hecho, las guías clínicas van en esa línea, dado que nos abren un montón de opciones y nosotros tenemos que ir buscando cuál es la opción más indicada para cada uno de los pacientes que tenemos delante.




