Redacción Farmacosalud.com
La Comisión Europea ha aprobado el uso de Bevacizumab (Avastin®) para el tratamiento del cáncer de cérvix avanzado. La indicación autorizada es en combinación con quimioterapia, bien paclitaxel más cisplatino, o bien paclitaxel más topotecan (si la paciente no puede recibir platino) en mujeres con cáncer recurrente o metastásico(1). De este modo, el antiangiogénico se puede convertir en la primera terapia biológica en incorporarse al arsenal terapéutico contra un tumor que apenas ha registrado avances en las últimas décadas y cuya incidencia se localiza sobre todo en edades entre los 35 y los 44 años(2). En la Unión Europea, se estima que cada día se diagnostican 90 casos de cáncer de cérvix y cerca de 35 fallecerá por esta causa(3). En España la cifra es de unos 2.100 diagnósticos anuales, ha informado la compañía Roche.
Como ya sucediera con la aprobación de la FDA el pasado mes de agosto, la autorización se ha basado en los datos del estudio fase III GOG-0240. España, con 6 hospitales y 18 pacientes, es el único país europeo que ha participado en esta investigación del Grupo de Oncología Ginecológica (GOG), que cuenta con el apoyo del Instituto Nacional del Cáncer de Estados Unidos (NCI). Esta indicación también fue aprobada el año pasado en Suiza y en otros seis países. El ensayo clínico cumplió su objetivo primario al demostrar un aumento estadísticamente significativo de la supervivencia entre las mujeres tratadas con Bevacizumab en combinación con quimioterapia frente a aquellas que fueron tratadas únicamente tratadas con quimioterapia. Concretamente las pacientes experimentaron una reducción del riesgo de muerte estadísticamente significativa del 29%, lo que supuso un incremento de la mediana de supervivencia de cerca de 4 meses respecto a las tratadas solo con quimioterapia (mediana de supervivencia global: 17,0 meses frente a 13,3 meses; hazard ratio [HR]=0,71, p=0,004)(1).
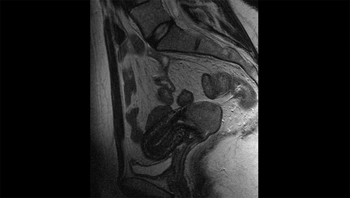
Cáncer cervical o de cérvix visto mediante una imagen por resonancia magnética sagital de la pelvis
Autor/a de la imagen: (my own work)
Ca cervicis uteri T2 SAG de my own work - Trabajo propio. Disponible bajo la licencia CC BY-SA 3.0 vía Wikimedia Commons - http://commons.wikimedia.org/wiki/File:Ca_cervicis_uteri_T2_SAG.jpg
#/media/File:Ca_cervicis_uteri_T2_SAG.jpg
Fuente: Wikipedia / Rádiológ
Escasez de opciones terapéuticas disponibles para el cáncer de cérvix
El GOG-0240 es un estudio independiente fase III, que determinó el perfil de eficacia y seguridad de Bevacizumab más quimioterapia (paclitaxel y cisplatino o paclitaxel y topotecan) en mujeres con cáncer de cérvix avanzado o recurrente. El estudio, en el que participaron 452 pacientes, mostró también los siguientes resultados:
-La tasa de mujeres que recibieron Bevacizumab más quimioterapia y que experimentaron una reducción del tamaño del tumor (tasa de respuesta objetiva) fue claramente mayor que la observada entra las que recibieron solo quimioterapia [48% vs. 36%, p=0,008)(1).
-El perfil de seguridad de Bevacizumab fue similar al reportado en otros tumores, excepto por una mayor incidencia de fístulas gastrointestinales-vaginales en las pacientes que recibieron Bevacizumab y quimioterapia que en las tratadas únicamente con quimioterapia (6% vs. <1%, respectivamente). En todos estos casos las afectadas habían recibido radioterapia pélvica previa(1).
El cáncer de cérvix, cuya incidencia anual en España es de unos 2.100 casos, está considerado una necesidad médica no cubierta por la escasez de opciones terapéuticas disponibles. Se calcula que este año se diagnosticarán en la Unión Europea más de 33.000 nuevos casos y unas 13.000 mujeres fallecerán por esta enfermedad(3). Las tasas de supervivencia difieren de forma sustancial según la fase en que se detecte la enfermedad: tras un diagnóstico en el estadio inicial, se calcula que el 90% sobrevive al cabo de cinco años, pero la cifra baja al 15-20% si el tumor metastatiza(2,4). A nivel mundial se estima que cada año se diagnostican más de medio millón de tumores(4) y se producen más de 260.000 muertes, siendo la cuarta causa de fallecimiento por cáncer en mujeres(5).
Bevacizumab bloquea un elemento esencial en la angiogénesis
La angiogénesis es el proceso a través del cual un tumor induce la creación de nuevos vasos sanguíneos que le permitan seguir creciendo. Cuando su tamaño supera el milímetro necesita desarrollar su propia red de vasos que le aporten los nutrientes necesarios. Bevacizumab actúa bloqueando un elemento esencial en este fenómeno: el receptor del factor de crecimiento endotelial vascular (VEGF, por sus siglas en inglés). El VEGF juega un papel clave en la progresión de diferentes tumores; de hecho Avastin® tiene indicaciones aprobadas en cáncer colorrectal, mama, pulmón, riñón y ovario.
Referencias
1. Ficha Técnica del producto
2. National Cancer Institute. Surveillance, Epidemiology and End Results program (SEER) Stat Fact Sheets: Cervix Uteri Cancer. Last accessed March 2015 at http://seer.cancer.gov/statfacts/html/cervix.html
3. European Cancer Observatory: Cancer Incidence, Mortality, Prevalence and Survival in Europe. Cervical cancer. Last accessed. March 2015 at http://eco.iarc.fr/eucan/CancerOne.aspx?Cancer=25&Gender=2
4. Mayo Clinic. Cervical cancer symptoms. Last accessed March 2015 at http://www.mayoclinic.org/diseases-conditions/cervicalcancer/ basics/symptoms/con-20030522
5. GLOBOCAN 2012: Estimated Cancer Incidence, Mortality and Prevalence Worldwide in 2012. Last accessed March 2015 at http://globocan.iarc.fr/Pages/fact_sheets_population.aspx
6. Tewari K et al. N Eng J Med 2014;370(8):734-43




