Artículo de la Dra. Amparo Marco Martínez
INTRODUCCIÓN
En la diabetes mellitus tipo 2 (DM 2) múltiples mecanismos contribuyen al desarrollo de la hiperglucemia; la resistencia a la insulina a nivel de tejido muscular, hepático y en adipocitos asociada a anormalidades en la producción y secreción de insulina se han propuesto como los mecanismos principales, pero se conocen hasta ocho anormalidades metabólicas y hormonales implicadas.(1) El tratamiento de la DM 2 es a menudo complicado por la coexistencia de obesidad, que además contribuye a empeorar la acción de la insulina y agrava la hipertensión, hiperlipemia, inflamación y otros factores patogénicos que promueven el riesgo cardiovascular.

Doctora Amparo Marco
Fuente: Dra. Marco
Aunque en el manejo de la DM2 disponemos de múltiples opciones terapéuticas, cerca del 50% de los pacientes diabéticos no consiguen los objetivos de control glucémico deseados o éstos no se mantienen a largo plazo.(2,3) Por esta razón son necesarios nuevos fármacos que ofrezcan mecanismos de acción complementarios y que presenten una eficacia adicional a los ya existentes, con perfiles de seguridad favorables y beneficios sobre la obesidad y otros factores de riesgo cardiovascular.(2,3)
El riñón juega un papel importante en la homeostasis de la glucosa y recientemente se ha convertido en una diana terapéutica en la diabetes. En este artículo revisaremos el mecanismo de acción, eficacia y seguridad de los inhibidores de SGLT2, un nuevo grupo terapéutico que inhibe la reabsorción de glucosa en el túbulo contorneado proximal.
EL RIÑÓN Y LA HOMEOSTASIS DE GLUCOSA
El riñón interviene en la regulación de la homeostasis de la glucosa por tres mecanismos diferentes; liberación de 15-55 g glucosa a la circulación (gluconeogénesis), captación de glucosa de la circulación para suplir sus necesidades energéticas (25-35 g/día) y la más importante: la reabsorción de glucosa procedente del filtrado glomerular.(3-5) Todos estos mecanismos están alterados en pacientes con DM2.
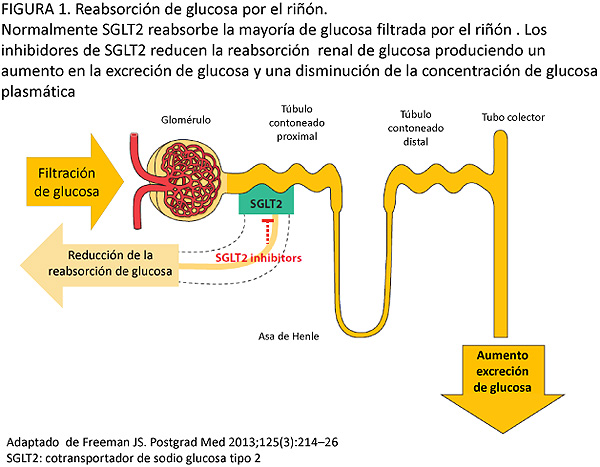
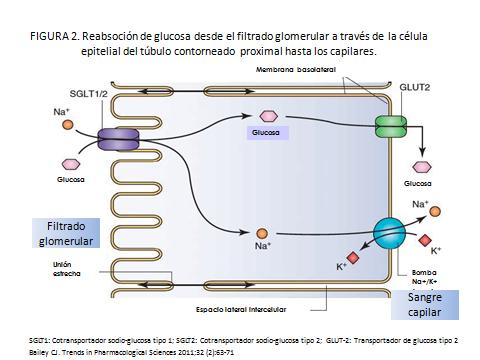
Normalmente, el riñón filtra aproximadamente 180 litros de plasma y 180 g de glucosa al día (ya que la concentración media de glucosa es de 100 mg/dl). En individuos sanos toda la glucosa filtrada es reabsorbida y la orina está libre de glucosa. Esta reabsorción de glucosa se produce por la acción de los co-transportadores sodio-glucosa (SGLT 1 y SGLT2) en el túbulo contorneado proximal. En condiciones normales, el 90% de la glucosa es reabsorbida en el segmento S1 y S2 del túbulo contorneado proximal por SGLT2, que es un co-transportador de alta capacidad y baja afinidad ubicado en las células epiteliales de la superficie luminal. El 10% restante se reabsorbe en el segmento S3 del túbulo contorneado proximal mediado por el co-transportador glucosa-galactosa (SGLT1) de alta afinidad y baja capacidad. SGLT1 se expresa también en intestino delgado y otros tejidos. La glucosa reabsorbida en el túbulo contorneado proximal se libera a la circulación por la acción de los facilitadores del transporte de glucosa (GLUT s) localizados en la membrana basolateral de las células epiteliales del túbulo contorneado proximal. (3-5) FIGURA 1 y 2.
Fuente: Dra. Marco
Fuente: Dra. Marco
En pacientes con diabetes se produce un aumento de la reabsorción de glucosa debido a un aumento del transporte máximo de glucosa relacionado con un aumento en la expresión génica de los tranportadores de glucosa, lo que contribuye al mantenimiento de la hiperglucemia. (3-5)
INHIBIDORES DE SGLT2. UN NUEVO GRUPO TERAPÉUTICO
La inhibición farmacológica de SGLT2 aumenta la excreción urinaria de glucosa (EUG) y disminuye la glucemia plasmática por un mecanismo de acción independiente de la insulina. Los inhibidores de SGLT2 representan una nueva clase terapéutica disponible recientemente para el tratamiento de la DM2 que han demostrado eficacia y efectos beneficiosos sobre otras comorbilidades asociadas a DM2 como la obesidad y la HTA.(5)
En la década de 1980, Rossetti y colaboradores(6) introdujeron el concepto de normalización de las concentraciones de glucemia por el incremento de la excreción urinaria de glucosa (EUG). Los autores mostraron que la floricina, un inhibidor no específico de SGLT1 y SGLT2, derivada de la corteza del manzano (descubierta en 1835) incrementaba la EUG y reducía la glucemia en ratas parcialmente pancreatectomizadas. Sin embargo, no se pudo utilizar para el tratamiento de la diabetes por presentar algunas limitaciones, pues tiene efecto inhibidor de SGLT 1 en el intestino, lo que provoca malabsorción de glucosa-galactosa así como diarrea, ofrece una baja biodisponibilidad por la degradación de las glucosidasas intestinales y además su metabolito bloquea el facilitador del transporte de glucosa GLUT 1, lo que podría interferir en la absorción de glucosa en algunos tejidos. (3,5,7)
Posteriormente se desarrolló la dapagliflozina, un inhibidor altamente selectivo de SGLT2 que fue aprobado para su utilización por la Agencia Europea del medicamento en 2012 y por la Food and Drug Administration (FDA) en Estados Unidos en enero de 2014. Más recientemente en Europa han sido aprobadas para su utilización la canagliflocina y empagliflocina, y otras moléculas se encuentran en fase de desarrollo.(5)
Este grupo de fármacos es muy atractivo por diferentes razones. Su mecanismo de acción es independiente de la función de la célula beta pancreática que se deteriora progresivamente y asocia pocos episodios de hipoglucemia. El efecto glucosúrico (60-80g de glucosa al día) se traduce en una pérdida calórica de aproximadamente 200-300 Kcal/día y una reducción de peso de 2,5-3,4 kg.(1,3,8) En los ensayos clínicos se demuestra una reducción en la tensión arterial por mecanismos no totalmente aclarados pero en el que interviene el efecto natriurético de los inhibidores de SGLT2 debido al mecanismo de cotransporte de sodio, la diuresis osmótica inducida por la glucosa, y se sugiere una inhibición del sistema renina-angiotensina-aldosterona secundario al aumento del aporte de sodio y al aporte yuxtaglomerular que se puede presentar con el uso de inhibidores de SGLT2, pero aún falta mayor evidencia científica.(5,9)

Autor/a: Amitchell125 (English Wikipedia)
Fuente: Wikimedia Commons
EFICACIA
Dapagliflozina es el inhibidor de SGLT2 del que más ensayos clínicos se han publicado. Su eficacia se ha demostrado en monoterapia y en combinación con otros antidiabéticos orales o insulina en más de 9.000 pacientes con DM2.(3,5,8) Aunque no existen estudios directos, los datos de eficacia obtenidos con otros inhibidores de SGLT2 (canagliflocina y empagliflocina) son similares.(3) La reducción de HbA1c, cuando se compara con placebo, se encuentra entre 0.5-0.9 % y la de glucemia basal entre 15 -28 mg/dl.(5,8) Este efecto hipoglucemiante es independiente del tiempo de evolución de la enfermedad, pues se confirma tanto en pacientes de más de 10 años de evolución como en menos de 10 años de evolución, se produce de forma inmediata y, tal y como demuestran los ensayos clínicos en fase III, se mantiene durante más de dos años.(9,10,12) Como era de esperar, la reducción de HbA1c es mayor en pacientes con peor control metabólico inicial.(11)
EFECTO SOBRE OTROS FACTORES DE RIESGO CARDIOVASCULAR
Efectos sobre el peso
El efecto hipoglucemiante se acompaña de una pérdida de 2-3 kilos de peso por el efecto glucosúrico ya que, como hemos mencionado previamente, la glucosuria de 60-80 g/día lleva asociada una pérdida calórica de 200-300 Kcal/día. Al igual que ocurre con la mejoría del control metabólico, la pérdida de peso se mantiene a los cuatro años de iniciado el tratamiento.(3,5,10) En los estudios de composición corporal se observa que esta reducción ponderal se produce sobre todo a expensas de la masa grasa, particularmente tejido adiposo visceral.(12)
Efectos sobre la tensión arterial (TA)
Los inhibidores de SGLT2 producen una disminución de la TA sistólica de 3-9 mmHg, tanto en pacientes hipertensos como no hipertensos. La reducción en la TA diastólica es menos llamativa. Esta disminución de la TA no se acompaña de fenómenos de ortostatismo.(3,5) Como se ha comentado, el mecanismo no está totalmente aclarado pero la diuresis osmótica y el efecto natriurético juegan un papel importante en esta reducción.
Efectos sobre los lípidos
Los inhibidores de SGLT2 no parece que actúen directamente sobre el metabolismo de los lípidos y su efecto sobre los mismos es insignificante. Se pueden observar ligeros aumentos de los niveles de HDL (2%) y reducción de triglicéricos (4.7%), así como un aumento de LDL (0.8%) sin cambios en el ratio LDL/HDL.(3,5)
El análisis de los eventos cardiovasculares mayores (MACE: muerte cardiovascular, infarto de miocardio no fatal e ictus no fatal) ocurridos durante los ensayos clínicos muestran una reducción de eventos con dapagliflozina. La reducción de la hiperglucemia, la pérdida de peso y reducción de la TA podrían contribuir a esta observación. En la actualidad se están llevando a cabo estudios prospectivos de seguridad cardiovascular con canagliflocina (CANVAS) que incluye 4.400 pacientes y dapagliflozina (DECLARE) que incluye 17.000 pacientes y cuyos resultados podrán aportar más información sobre seguridad cardiovascular. (3)
SEGURIDAD
En los ensayos clínicos se observa que los inhibidores de SGLT2 son fármacos bien tolerados tanto en monoterapia como en asociación con otros agentes y los efectos adversos reportados ocurren con una frecuencia similar a placebo, excepto los observados para las infecciones genitourinarias; tanto es así, que el grado de abandonos mostrado en los ensayos clínicos fue excepcional. Las hipoglucemias son infrecuentes, similares a placebo, salvo cuando se asocian al tratamiento con insulina o sulfonilureas. En este caso se recomienda reducir la dosis de las mismas cuando se inicia tratamiento con inhibidores de SGLT2.(3)

Autor/a: Lockhear
Fuente: www.fotocommunity.com / Creative Commons
El exceso de excreción urinaria de glucosa que acompaña a la inhibición de SGLT se puede acompañar de un incremento en las infecciones genitales (vulvo vaginitis y balanitis), sobre todo en mujeres (5,5% en pacientes tratados con dapagliflozina y 0,6% con placebo) y un modesto incremento de las infecciones urinarias, pero no significativamente diferentes a los pacientes tratados con placebo. La mayoría de las infecciones fueron leves o moderadas en intensidad y respondieron al tratamiento antimicrobiano estándar.(3,5) No se observó aumento del riesgo de infecciones severas o pielonefritis.
Aunque el tratamiento con inhibidores de SGLT2 no demostró efecto carcinogenético en estudios preclínicos y no se detectó aumento en el número total de tumores en el desarrollo clínico, se observó un aumento en el número de tumores de mama, próstata y vejiga en los ensayos clínicos. Estos cánceres se identificaron tempranamente en los ensayos clínicos, lo que unido a la ausencia de receptores SGLT2 a estos niveles limita la posibilidad de que se hubieran desarrollado en el período de randomización. Por otra parte, la atención prestada en los ensayos clínicos a la pérdida de peso pudo permitir la detección de cánceres de mama preexistentes, las molestias urinarias podrían indicar problemas prostáticos previos y la hematuria no resuelta identificar cáncer de vejiga.(3,13)
OTRAS CONSIDERACIONES
No se recomienda iniciar el tratamiento con inhibidores de SGLT2 en pacientes con enfermedad renal moderada o severa (FGE <60 m/min) o en pacientes en diálisis, ya que la eficacia de estos fármacos depende de la existencia de una adecuada filtración de glucosa que no se cumple en pacientes con insuficiencia renal; sin embargo, no es necesario ajuste de dosis en pacientes con insuficiencia renal leve.(3,5)
La depleción de volumen debida a la diuresis osmótica puede causar hipovolemia, hipotensión y deshidratación y por ello no se recomienda su uso en pacientes que se encuentran en tratamiento con diuréticos de asa ni en situaciones de depleción de volumen.
Debido a la experiencia limitada en pacientes mayores de 75 años no se recomienda su uso.
QUÉ LUGAR OCUPAN LOS INHIBIDORES DE SGLT2 EN EL TRATAMIENTO DE LA DM 2
Dado que la inhibición de SGLT2 reduce la hiperglucemia por una vía independiente de la insulina, este nuevo grupo terapéutico se propone como una herramienta útil en toda las fases de la historia natural de la enfermedad, siempre que la función renal esté conservada, y tanto en monoterapia como en asociación a otros fármacos hipoglucemiantes o insulina.
El escenario más adecuado sería la utilización en pacientes con sobrepeso u obesidad que no estén controlados con metformina u otros fármacos hipoglucemiantes, especialmente cuando hay riesgo de hipoglucemias, y comorbilidades asociadas a la obesidad como la apnea del sueño o hipertensión arterial severa. Se puede utilizar también como triple terapia si la función renal lo permite.(3)
En estos momentos ya se incluye en los algoritmos de tratamiento de las sociedades científicas internacionales como la Sociedad Americana de Diabetes (ADA) (14) publicados recientemente y con anterioridad las recomendaciones de la Sociedad Americana de Endocrinólogos Clínicos (AACE) (15), la posibilidad de utilizar los inhibidores de SGLT2 como segundo escalón terapéutico cuando con metformina no se consigue el objetivo de control deseado; sobre todo, en pacientes con riesgo de hipoglucemia y con sobrepeso u obesidad. FIGURA 3.
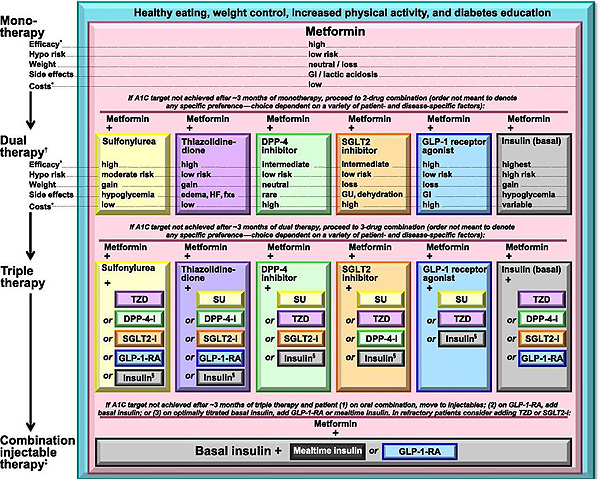
FIGURA 3. Algoritmo de tratamiento hipoglucemiante. ADA 2015
Approaches to Glycemic Treatment. Diabetes Care 2015; 38 (suppl 1): S43
Figura 7.1; adapted with permission from Inzucchi SE, et al. Diabetes Care, 2015: 140-149
Fuente: Dra. Marco
Dapagliflozina está disponible en comprimido de 10mg que se administran una vez al día con independencia de las comidas.
CONCLUSIONES
Los inhibidores de SGLT2 son un nuevo grupo de fármacos antidiabéticos que ha demostrado eficacia hipoglucemiante, tanto a corto como a largo plazo, y mejoría de otras comorbilidades asociadas a la diabetes como el sobrepeso, la obesidad y la HTA cuando se utilizan en monoterapia o asociados a otros antidiabéticos orales o insulina. Ello ocurre por un mecanismo de acción en el que el riñón juega un papel decisivo al actuar inhibiendo la reabsorción de glucosa en el túbulo contorneado proximal.
Puesto que la acción es independiente de la insulina, el riesgo de hipoglucemias es bajo y se pueden utilizar en todos los momentos evolutivos de la enfermedad. Esto hace que se proponga su utilización en pacientes con función renal normal en los que la metformina no permite conseguir los objetivos metabólicos planteados y sobre todo en pacientes con sobrepeso u obesidad o en los que se pretenda evitar el riesgo de hipoglucemias.
La mayor desventaja del tratamiento con inhibidores de SGLT2 es el aumento del riesgo de infecciones genitourinarias, especialmente en mujeres.
Su utilización en situaciones de práctica clínica habitual permitirá conocer más datos sobre la seguridad a largo plazo.
BIBLIOGRAFÍA
1. De Fronzo RA. From triumvirate to the ominous octet: a new paradigm for the treatment of type 2 diabetes mellitus. Diabetes. 2009; 59: 773-95.
2. Bailey CJ, Del Prato S, Barnett AH, Tahrani AA. Management of type 2 diabetes: new and future developments in treatment. Lancet. 2011; 378: 182-97.
3. Tahrani AA, Barnett AH, Bailey CJ. SGLT inhibitors in management of diabetes. Lancet Diabetes Endocrinol. 2013;1: 140-51.
4. DeFronzo R A, Davidson, J A , Del Prato, S.The role of the kidneys in glucose homeostasis: a new path towards normalizing glycaemia. Diabetes obes metab. 2012; 14:5-14.
5. Farhad M Hasan, Mazen Alsahli, John E. Gerich. SGLT2 inhibitors in the treatment of type 2 diabetes. Diabetes Research and Clinical Practice.2014; 104:297-322.
6. Rossetti L, Smith D, Shulman GI, Papachristou D, DeFronzo RA. Correction of hyperglycemia with phlorizin normalizes tissue sensitivity to insulin in diabetic rats. J Clin Invest. 1987;79: 1510-15.
7. Ehrenkranz JR, Lewis NG, Kahn CR, Roth J. Phlorizin: a review. Diabetes Metab Rev. 2005; 1: 31-38.
8. List JF, Woo V, Morales E, Tang W, Fiedorek FT. Sodium-glucose cotransport inhibition with dapagliflocin in type 2 diabetes.Diabetes Care. 2009;32:650-7.
9. Ferranini E, Solini A. SGLT2 inhibition in diabetes mellitus: rationale and clinical prospects. Nat Rev Endocrinol. 2012;8:495-502.
10. Bailey CJ, Gross JL, Hennicken D, Iqbal N, Mansfield TA, List JF. Dapagliflocin add-on to metformin in type 2 diabetes inadequately controlled with metformin: a randomised, double blind, placebo- controlled102 week trial. BMJ Med. 2013;11:43.
11. Zhang L, Feng Y, List J, Kasichayanula P, Pfister M. Dapagliflocin treatment in patients with different stages of type 2 diabetes mellitus. Diabetes Obes Metab. 2010;12(6):510-16.
12. Bolinder J, Ljunggren O, Kullberg J, et al. Effects of dapagliflocin on body weight, total fat mass, and regional adipose tissue distribution in patients with type 2 diabetes mellitus with inadequate glycemic control on metformin. J Clin Endocrinol Metab. 2012;97(3):1020-31.
13. Bailey CJ. Interpreting adverse signals in diabetes drug development programs. Diabetes Care. 2013;36:2098-106.
14. Standards of Medical Care in Diabetes—2015.Diabetes Care. 2015;38:S41-S48.
15. AACE Comprehensive Diabetes Manegement Algohoritm. Endocr Pract. 2013;19(Suppl 2): 19.




