Redacción Farmacosalud.com
Bajo el título ‘6 preguntas prácticas sobre mieloma múltiple. El papel del farmacéutico hospitalario‘, www.farmacosalud.com acogió un webinar formativo que contó con la presencia como moderador del Dr. Miguel Ángel Calleja, miembro del Servicio de Farmacia Hospitalaria del Hospital Virgen Macarena (Sevilla), y como ponentes de las Dras. María Victoria Mateos, facultativa del Servicio de Hematología del Complejo Hospitalario de Salamanca, y Estela Moreno, adscrita al Servicio de Farmacia Hospitalaria del Hospital de Sant Pau (Barcelona). La sesión, patrocinada por Amgen, GSK y Sandoz, estuvo avalada por la Sociedad Española de Farmacia Hospitalaria (SEFH). Cada ponente contestó a 3 del total de 6 interrogantes planteados. La Dra. Mateos aseguró en su exposición que, hoy en día, las nuevas opciones terapéuticas para el mieloma múltiple (MM) están permitiendo cubrir necesidades médicas no resueltas en pacientes triple-refractarios.

Fuente: www.farmacosalud.com
Dra. María Victoria Mateos
1. ¿Qué hacer en los casos de MM refractario y recidivante a varias líneas de tratamiento?
Los inhibidores de proteasoma y los fármacos inmunomoduladores, y posteriormente los anticuerpos monoclonales antiCD38, han sido los pilares del tratamiento frente al mieloma múltiple (MM). Todos estos fármacos han aportado mejoras en supervivencia global, “pero es cierto que cada vez nos encontramos antes con pacientes que ya han sido expuestos a los inhibidores de proteasoma, a los inmunomoduladores y los anticuerpos monoclonales antiCD38, porque cada vez combinamos más este tipo de fármacos y los movemos hacia líneas más precoces”, señaló la Dra. Mateos.
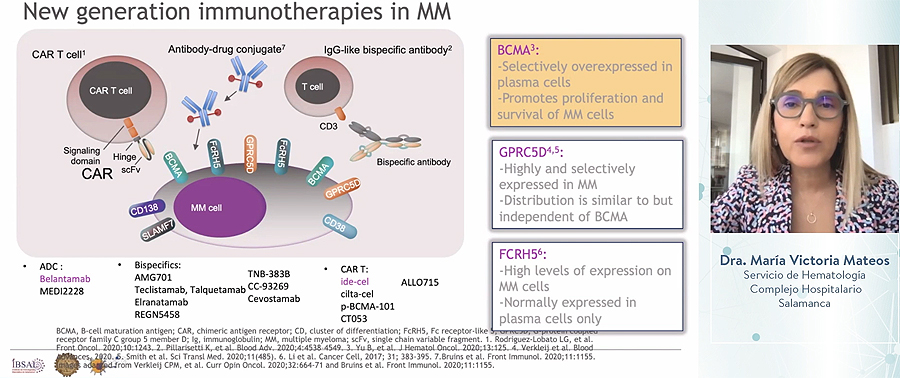
La mayoría de sujetos expuestos a esas tres clases de medicamentos son refractarios al menos a los inmunomoduladores y a los anticuerpos antiCD38. La falta de un estándar de tratamiento para rescatar a estos enfermos va quedando paliada con la llegada de una nueva generación de fármacos, las inmunoterapias centradas en la diana BCMA. Este antígeno puede ser terapéuticamente atacado mediante anticuerpos monoclonales conjugados, anticuerpos bioespecíficos y linfocitos T-CAR (o CAR-T).
Difusión: www.farmacosalud.com
Belantamab mafodotin es un anticuerpo monoclonal conjugado que, usado en monoterapia, logra que 1 de cada 3 pacientes de MM responda al tratamiento, siendo la mayoría de las respuestas “de calidad”, argumentó Mateos, quien destacó también la importancia de que la duración de la respuesta sea de aproximadamente 1 año y que la supervivencia global sea superior al año. Si bien belantamab mafodotin “cubre la necesidad médica no cubierta que teníamos para estos pacientes triple-refractarios”, también hay que decir que produce toxicidad ocular, algo común a los anticuerpos monoclonales conjugados, explicó la Dra. Mateos. Con todo, se trata de “una queratopatía manejable”, detalló.
Ide-cel es un CAR-T frente a BCMA. En individuos triple-refractarios, ide-cel ha permitido obtener tasas de respuesta superiores al 70%, con un 33% de remisiones completas, una supervivencia libre de progresión de 9 meses y una supervivencia global cercana a los 2 años. “Por lo tanto -aseveró la experta-, de nuevo también se cubre la necesidad médica no cubierta”. La aplicación de ide-cel presenta asimismo un perfil de toxicidad nuevo, como es el síndrome de liberación de citoquinas, la neurotoxicidad y la toxicidad hematológica.
Cilta-cel, el segundo linfocito T-CAR frente a BCMA, será aprobado próximamente por la Agencia Europea del Medicamento. De acuerdo con la Dra. Mateos, los datos reportados hasta ahora con este tratamiento en individuos triple-refractarios “son realmente esperanzadores”, dado que la aplicación de cilta-cel se asocia con una tasa de remisiones completas que llega al 83%. Además, más del 60% de los pacientes permanecen vivos y libres de progresión de la afección a 2 años, con un perfil de seguridad similar al descrito para ide-cel.
En conclusión, todas estas terapias “cubren la necesidad médica no cubierta que tenemos para los pacientes triple-refractarios”, afirmó la facultativa. “Los anticuerpos bioespecíficos vendrán posteriormente”, añadió.
2. ¿Existe una secuencia de tratamientos y líneas terapéuticas más ventajosa en MM?
“Perdemos un tercio de los pacientes entre la primera y la segunda línea, y entre la segunda y las siguientes líneas de tratamiento. Y esto es aplicable tanto a pacientes jóvenes como a pacientes mayores… quizás un poquito más acusado si cabe en la población de pacientes mayores. Por ello, el primer concepto importante es que tenemos que intentar utilizar las mejores combinaciones como parte de la primera línea de tratamiento”, destacó la facultativa del Complejo Hospitalario de Salamanca.
Actualmente, se están incorporando los anticuerpos monoclonales antiCD38 como parte de la primera línea de tratamiento para el MM. Sin embargo, en el momento de la recaída, la mayoría de enfermos han sido expuestos a inhibidores de proteasoma e IMiD’s (inmunomoduladores), siendo la mayor parte de los sujetos refractarios a lenalidomida. Por lo tanto, hay que plantear una secuencia de tratamiento que se adapte a esta situación. La primera pregunta que debe hacerse el médico es si el paciente ha recibido antiCD38:
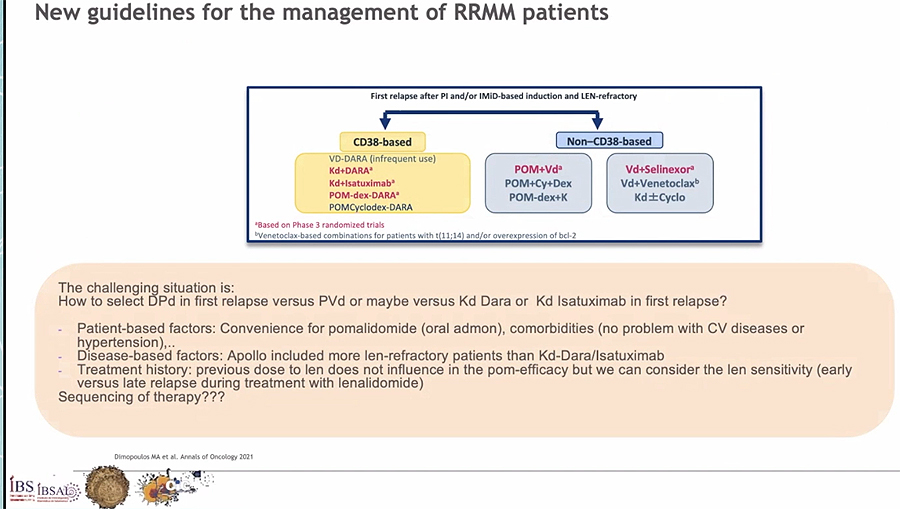
Kd: carfilzomib-dexametasona; DARA: daratumumab; POM: pomalidomida
Difusión: www.farmacosalud.com
La secuencia de tratamiento óptima pasa por incorporar cada vez más en primera línea inhibidores de proteasoma, IMiD’s y antiCD-38, pero la realidad es que hoy por hoy la mayoría de pacientes en recaída todavía no han sido expuestos a antiCD38, y por lo tanto “la secuencia óptima sería elegirlo”, dijo la Dra. Mateos. Si se viene de ser refractario a lenalidomida -la mayoría de casos-, “la situación óptima es elegir el inhibidor de proteasoma, y si no se es candidato, elegiríamos el inmunomodulador pomalidomida”, especificó. “Mencionar venetoclax probablemente en el futuro para pacientes con traslocación 11;14... y ya para las siguientes líneas entra en juego la terapia frente a BCMA con belantamab mafodotin o los linfocitos T-CAR como opciones más realistas en el futuro cercano”, adujo la hematóloga.
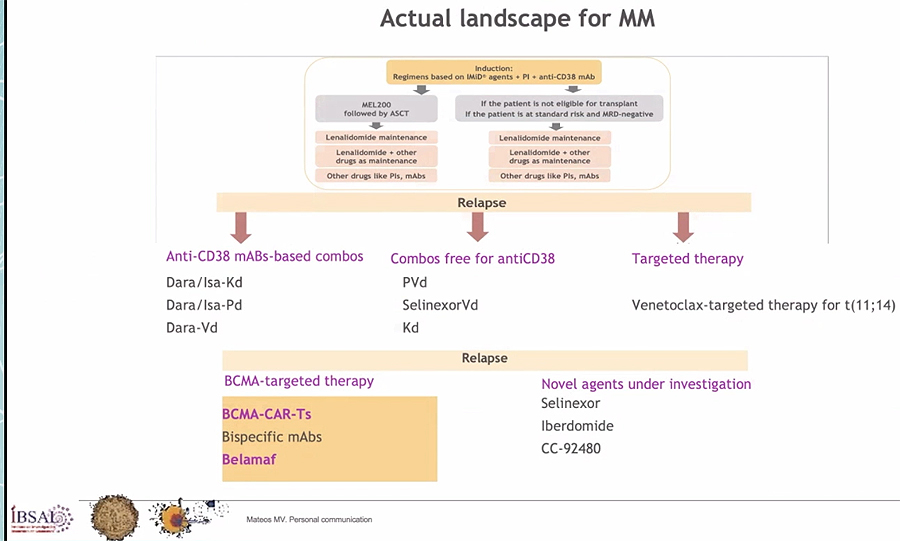
Difusión: www.farmacosalud.com
3. ¿Qué ventajas tiene un tratamiento en monoterapia en MM?
El mieloma múltiple sigue siendo una patología incurable para la mayor parte de las personas afectadas, quienes, estando sometidas a ciclos de remisión y de recaída, pueden llegar a recibir hasta 6 líneas de tratamiento. El MM afecta fundamentalmente a gente de edad avanzada (la edad media al diagnóstico son 69 años). Dada la complejidad de la enfermedad desde el punto de vista patogénico (las células plasmáticas evolucionan en un modelo en ‘ramas’, el tratamiento influye en la selección clonal y hay de por medio elementos de micro-medioambiente), en principio los médicos tienden a utilizar combinaciones de fármacos. Según Mateos, la mayoría de los nuevos fármacos para el MM son evaluados en fases avanzadas de la enfermedad y, como medicamentos únicos, ahí están “los nuevos CELMoDs, iberdomida, CC480 y selinexor + dexametasona”, así como los linfocitos T-CAR, belantamab mafodotin y, dentro de un tiempo, los bioespecíficos.
Si bien es cierto que en fases avanzadas del MM los fármacos se evalúan habitualmente en monoterapia -y esto ha sido así para todos los medicamentos-, “el siguiente paso, por supuesto, será combinarlos”, avanzó la especialista. A juicio de la Dra. Mateos, por ahora el perfil ideal para recibir el modelo de fármaco único se corresponde con un anciano cuya MM esté ya en una etapa bastante evolucionada. En estos casos, el objetivo del tratamiento será controlar la patología con un perfil de seguridad terapéutica “aceptable”, subrayó.

Difusión: www.farmacosalud.com
Si se quiere conocer con detalle la ponencia de la Dra. Mateos, entrar en la grabación que sigue a continuación (clicar aquí o sobre la imagen):




