Redacción Farmacosalud.com
La Comisión de Salud Pública del Ministerio de Sanidad y Consumo de España ha aprobado la incorporación de los niños de entre 5 y 11 años a la Estrategia Nacional de vacunación frente al COVID-19, con el propósito de disminuir la carga de enfermedad de este colectivo y la transmisión en el entorno familiar, en los centros educativos y en la comunidad. En este sentido, la Comisión destaca la importancia de proteger a los menores de estas edades no sólo de la enfermedad en su faceta aguda, sino también ante posibles afecciones a futuro y frente al síndrome de COVID Persistente. Actualmente, en España hay censados unos 3,3 millones de niños de estas edades que son susceptibles de recibir la protección frente al COVID-19. En este momento, los menores de 12 años constituyen el grupo de edad con mayor incidencia acumulada de casos de infecciones derivadas del coronavirus SARS-CoV-2. El análisis epidemiológico del COVID-19 en la población entre 5 y 11 años de edad durante la quinta onda pandémica en España, mostró que el 99,7% de los casos diagnosticados presentaron un cuadro leve, siendo la mitad de ellos incluso asintomáticos. El 0,21% de los casos precisó hospitalización, y el 0,016% requirió ingreso en UCI (Unidad de Cuidados Intensivos) pediátrica.
El 25 de noviembre la Agencia Europea del Medicamento (EMA en sus siglas en inglés) ya autorizó la vacuna infantil Comirnaty BNT162B2 (Pfizer/BioNTech) para la población de entre 5 y 11 años. Este suero se dispensará en viales diferentes a los utilizados para la población adulta. Asimismo, la Comisión de Salud Pública, a instancia de la Ponencia de Vacunas, decidió que el intervalo de administración de la segunda dosis sea de 8 semanas, para contribuir a incrementar la respuesta inmune.
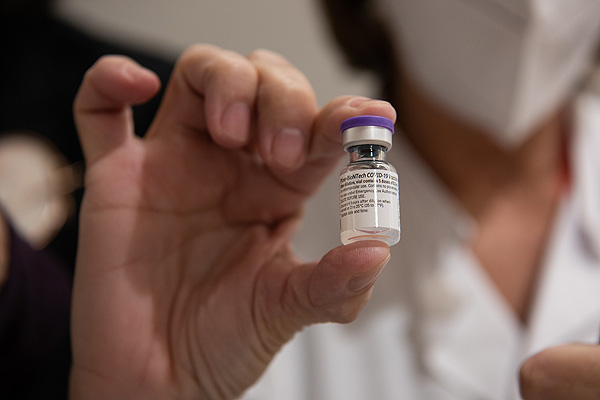
Vacunación frente al COVID-19
Autor/a de la imagen: Oriol Martí - Hospital Clínic
Fuente: Hospital Clínic de Barcelona
Con motivo del inicio de la campaña de vacunación infantil frente al COVID-19 que comienza este 15 de diciembre, el Comité de Alergia Infantil de la Sociedad Española de Alergología e Inmunología Clínica (SEAIC) ha elaborado las siguientes recomendaciones para los niños con alergia de entre 5 y 11 años:
¿Cuál es el riesgo de reacciones alérgicas a la vacuna frente al COVID-19?
En el ensayo clínico de la vacuna Comirnaty BNT162b2 (Pfizer/BioNTech) en el grupo de edad de 12 a 15 años no hubo informes de reacciones alérgicas graves. Los eventos adversos descritos con más frecuencia tras la administración de la vacuna frente al SARS-CoV-2 son leves (aproximadamente 1 de cada 10 personas que la reciben) e incluyen: dolor en la zona de inyección (80%), cansancio (50%), dolor de cabeza (30%), enrojecimiento e hinchazón en el lugar de la inyección (20%), dolor muscular y escalofríos (10%). Estados Unidos e Israel, entre otros, han comenzado a vacunar a la población infantil de 5 a 11 años. En concreto, en Estados Unidos se han administrado más de 5 millones de dosis hasta ahora (a fecha 9 de diciembre). Si bien todavía no se dispone de un análisis de la seguridad del preparado vacunal tras su uso a gran escala y su relevancia en la vida real, hasta la fecha no se ha generado ninguna señal de alarma sobre la seguridad de la vacunación en estos niños.
Las reacciones alérgicas son poco frecuentes. Para la vacuna Comirnaty BNT162b2 (Pfizer/BioNTech) se han registrado 5 casos de reacciones anafilácticas por 1 millón de dosis administradas. Todos los casos de anafilaxia han sido tratados de manera eficaz y con una recuperación completa. Los signos de una reacción alérgica grave a la vacuna pueden incluir: dificultad respiratoria, urticaria o erupción cutánea, hinchazón de la cara y/o garganta, dificultad para tragar, palpitaciones y/o mareo.
¿Cuáles son las recomendaciones de vacunación para los niños con alergia?
No se puede generalizar la evitación de la vacuna en todos aquellos sujetos pediátricos que hayan tenido reacciones alérgicas graves con medicamentos y/o alimentos. La SEAIC recomienda que todo paciente que vaya a ser vacunado frente al coronavirus sea vigilado por personal sanitario el tiempo pertinente tras su administración:
a) Serán 15 minutos, como se define en ficha técnica para la población general.
b) Aumentado a 30 minutos para los que padecen alguna enfermedad alérgica común (pólenes, otras rinoconjuntivitis, alergia a alimentos o alergia a medicamentos entre otras) o historia familiar de alergia grave (anafilaxia).
c) Un tiempo de 60 minutos en el caso de tener antecedentes personales de anafilaxia, alergia grave a otras vacunas, mastocitosis u otras afecciones de los mastocitos.
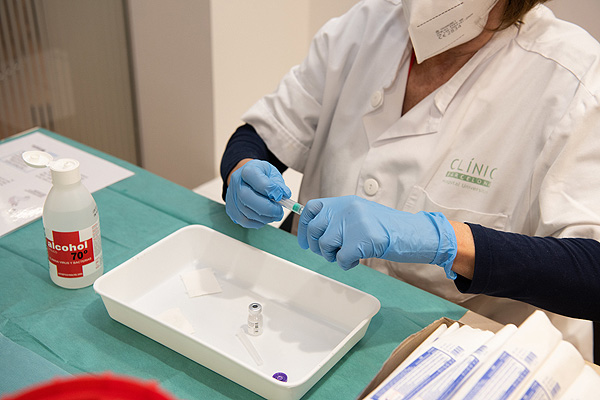
Vacunación frente al COVID-19
Autor/a de la imagen: Oriol Martí - Hospital Clínic
Fuente: Hospital Clínic de Barcelona (IMAGEN DE ARCHIVO)
Las reacciones alérgicas que pueden aparecer tras la administración de una vacuna dependerán de la composición de ésta (principio activo y excipientes). En general, las vacunas frente a los virus pueden variar en su composición tanto en el principio activo, como en sus excipientes:
a) como principio activo, la vacuna Comirnaty BNT162b2 (Pfizer/BioNTech) contiene 10 μg de ARNm, que codifica una proteína llamada S (spike) vehiculada en nanopartículas lipídicas de polietilenglicol entre otros componentes. La vacuna autorizada para niños de 5 a 11 años contiene un tercio del ARMm de las vacunas aprobadas para niños mayores y adultos (30 μg).
b) como excipientes, en el caso concreto de la vacuna Comirnaty BNT162b2, Pfizer/BioNTech), contiene POLIETINELGLICOL (PEG, que pueden estar presente en algunos cosméticos, geles de baños y medicamentos) y Trometamol (puede aparecer como excipiente en algunos fármacos). No contiene, sin embargo, trazas de huevo ni otros fármacos como antibióticos.
El suero Comirnaty BNT162b2 (Pfizer/BioNTech) no presenta, por lo tanto, más contraindicaciones en los niños alérgicos que cualquier otro niño de la población general. Como contraindicaciones figuran de forma absoluta solamente aquellos individuos que han sufrido reacciones alérgicas previas a sus componentes o aquellas que hayan presentado una reacción grave con la primera dosis de vacuna frente al coronavirus. Es importante destacar que la alergia a estos excipientes es excepcional en la población infantil.
¿Cuáles son las situaciones especiales con respecto a la vacunación frente al SARS-CoV-2 en la población de 5 a 11 años?
O La alergia a alimentos, aeroalérgenos, venenos de himenópteros o medicamentos, así como los tratamientos con corticoides inhalados para el asma o los corticoides tópicos para la dermatitis atópica, no contraindican la administración de la vacuna frente al SARS-CoV-2.
O Asma moderada o grave no controlada, o crisis de asma. Una vez controlada, el niño podría recibir la vacuna.
O Niños con inmunosupresión u otras alteraciones de la inmunidad. Según FACME, el niño puede recibir la vacuna teniendo en cuenta que es posible que la formación de anticuerpos no sea la óptima. Por tanto, el menor y su entorno deberán mantener las medidas de prevención de manera rigurosa.

Autor/a de la imagen: Enric Arandes
Fuente: E. Arandes / www.farmacosalud.com
O El angioedema hereditario y otras formas de angioedema no constituyen un riesgo para presentar un efecto secundario a la vacuna frente al SARS-CoV-2. La vacuna puede administrarse en los pacientes con dichas patologías con independencia del tratamiento de control que reciban para ellas.
O Niños con mastocitosis: se recomienda el pretratamiento con un antihistamínico H1 una hora antes de la administración de la vacuna y la vigilancia posterior en el centro sanitario durante 60 minutos.
O Coadministración con otras vacunas del calendario de vacunación infantil: las vacunas de ARNm frente al SARS-CoV-2 para población infantil se pueden administrar de manera concomitante con cualquier vacuna, en lugares anatómicos diferentes. Si no se aplican de forma concomitante, no es necesario esperar ningún intervalo entre los diferentes sueros. La protección óptima no se obtiene hasta trascurridos 7 días tras la administración de la segunda dosis de la vacuna.
Por lo tanto, la Sociedad Española de Alergología e Inmunología Clínica (SEAIC) concluye que:
O En los niños que hayan sufrido reacciones alérgicas graves por alimentos o medicamentos, no es necesario realizar de forma sistemática un estudio alergológico con la vacuna frente al SARS-CoV-2 previo a su administración.
O Sí deberá realizarse un estudio alergológico a posteriori en los niños que hayan sufrido reacciones alérgicas con la vacuna frente al SARS-CoV-2.

Actividad hospitalaria durante la crisis generada por el coronavirus
Fuente: Francisco Avia / Hospital Clínic de Barcelona (IMAGEN DE ARCHIVO)
Por último, el Comité de Alergia Infantil de la Sociedad Española de Alergología e Inmunología Clínica (SEAIC) se alinea con las recomendaciones propuestas por el Comité Asesor de Vacunas (CAV) de la Asociación Española de Pediatría (AEP) con relación a la vacunación de los niños frente al SARS-CoV-2:
1) Contemplar el derecho del niño a su protección individual frente a esta enfermedad que, aunque en general es leve en este grupo de edad, en ocasiones puede complicarse.
2) Fortalecer la inmunidad de grupo.
3) Disminuir la circulación del SARS-COV-2 y reducir la probabilidad de aparición de nuevas variantes que sean resistentes a las vacunas.
4) No privar a la población infantil del beneficio que aporta la inmunización, de la que ya gozan los mayores de 12 años, aunque los objetivos en términos de salud sean diferentes.
5) Conseguir y mantener espacios educativos seguros que permitan la normalización de la escolarización y las relaciones interpersonales de los niños en pro de su bienestar psicoemocional.




