Redacción Farmacosalud.com
La compañía Celgene ha presentado los resultados de los ensayos FIRSTTM y STRATUSTM en mieloma múltiple durante el 56º Congreso anual de la Sociedad Americana de Hematología (ASH), celebrado en San Francisco (EE.UU.). Cada año se diagnostican 144.000 casos nuevos en el mundo de este cáncer sanguíneo en el que las células plasmáticas -componentes importantes del sistema inmunológico- se reproducen de manera incontrolable y se acumulan en la médula ósea. El estudio FIRSTTM es un ensayo pivotal de fase III -también conocido como MM-020/IFM 07-01- en el que se compara la administración continua de REVLIMID® (lenalidomida) más una dosis baja de dexametasona (Rd continuo), con una duración fija de 18 ciclos de Rd (Rd18) o 12 ciclos de melfalán, prednisona y talidomida (MPT) para el tratamiento del mieloma múltiple recién diagnosticado, no candidato a trasplante. Como conclusión principal, el estudio alcanzó el criterio de valoración principal de supervivencia libre de progresión (SLP) en el análisis por intención de tratar de todos los pacientes aleatorizados (media de la SLP de 21,2 meses con MPT frente a 25,5 meses con Rd, cociente de riesgo (HR, Hazard Ratio) de 0,72, p<0,01). O sea, REVLIMID® (lenalidomida) continuo más dosis baja de dexametasona aumentó la supervivencia libre de progresión comparado con una duración fija de Rd o melfalán, prednisona y talidomida independientemente de la edad, insuficiencia renal o profundidad de la respuesta, han precisado fuentes de Celgene.
En el análisis, los autores examinaron la repercusión de la edad (75 años o menos frente a más de 75 años) en la SLP y en las variables secundarias del estudio. El 35% de los pacientes tenía más de 75 años de edad.
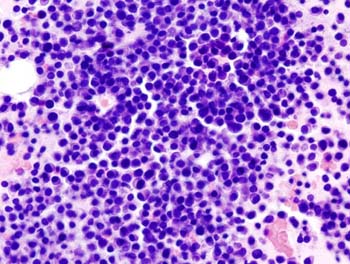
Mieloma múltiple: aspirado de médula ósea; tinción con hematoxilina-eosina
Autor/a de la imagen: «Multiple myeloma (2) HE stain». Publicado bajo la licencia CC BY-SA 3.0 vía Wikimedia Commons - http://commons.wikimedia.org/wiki/File:Multiple_myeloma_(2)_HE_stain.jpg mediaviewer/File:Multiple_myeloma_(2)_HE_stain.jpg.
Fuente: Wikipedia / KGH
Otros datos positivos:
- Las tasas de respuesta fueron mayores con Rd continuo frente a MPT y la duración de la respuesta fue mayor en el grupo de Rd continuo en comparación con MPT en ambos grupos de edad.
- Los resultados de SLP y supervivencia global (SG) favorecieron a Rd continuo sobre MPT y sobre Rd18 en ambos grupos de edad.
- Rd continuo demostró una SLP mayor en comparación con MPT en todos los grupos de pacientes con insuficiencia renal, en particular, en pacientes con función renal normal (HR = 0,71; P = 0,05), en pacientes con insuficiencia renal leve (HR = 0,74; P = 0,02), pacientes con insuficiencia renal moderada (HR = 0,66; P < 0,01) y en pacientes con insuficiencia renal grave (HR = 0,76; P=0,31). Se observó también un ligero beneficio en la SLP con el Rd continuo comparado con Rd18 (una comparación secundaria) en pacientes con insuficiencia renal leve o moderada (P < 0,01 para ambos). “Estos análisis siguen validando los datos publicados para ciertos pacientes de más edad que recibían tratamiento continuo con lenalidomida y dexametasona en comparación con el régimen del triplete estándar”, ha señalado el profesor Thierry Facon, MD, Universidad de Lille e investigador principal del estudio.
Los resultados de seguridad del estudio FIRST (N Engl J Med 2014) mostraron que los acontecimientos adversos de grado 3/4 que se dieron en al menos el 8% de los pacientes en el grupo de Rd continuo, grupo de Rd18 o grupo de MPT incluyeron neutropenia (28%, 26% y 45%, respectivamente), anemia (18%, 16% y 19%, respectivamente), trombocitopenia (8%, 8% y 11%, respectivamente), neutropenia febril (1%, 3% y 3%, respectivamente), leucopenia (5%, 6% y 10%, respectivamente), infección (29%, 22% y 17%, respectivamente), neumonía (8%, 8% y 6%, respectivamente), trombosis venosa profunda y/o embolia pulmonar (8%, 6% y 5%, respectivamente), astenia (8%, 6% y 6%, respectivamente), fatiga (7%, 9% y 6%, respectivamente), y neuropatía sensorial periférica (1%, < 1% y 9%, respectivamente). Las tasas de trastornos cardíacos de grado 3/4 en los pacientes de los grupos con Rd continuo, Rd18 y MPT fueron del 12%, 7% y 9%, respectivamente. La incidencia de segundos tumores primarios invasivos fue del 3% en pacientes que tomaban Rd continuo, del 6% en pacientes que tomaban Rd18 y del 5% en pacientes que tomaban MPT. La incidencia global de tumores sólidos fue idéntica en los grupos de Rd continuo y MPT (3%) y del 5% en el grupo de Rd18.

Autor/a: Petr Kratochvil
Fuente: www.publicdomainpictures.net
Principales datos del estudio STRATUSTM
Definición: STRATUSTM (MM-010) evalúa la seguridad de IMNOVID® (pomalidomida) más dosis baja de dexametasona en pacientes en recaída y refractarios con MM que anteriormente habían sido tratados sin éxito con lenalidomida y bortezomib. El STRATUSTM es un estudio fase IIIb de un único brazo con IMNOVID® (pomalidomida) más dosis baja de dexametasona en pacientes con MM -refractarios o en recaída - que anteriormente habían sido tratados con lenalidomida y bortezomib sin éxito. El objetivo primario fue evaluar la seguridad, mientras que el objetivo secundario clave analizó la exposición a pomalidomida, la tasa global de respuesta (TGR; ≥ respuesta parcial) y su duración, la supervivencia libre de progresión (SLP), la supervivencia global (SG) y el estudio citogenético. Los pacientes tenían una mediana de cinco tratamientos previos. Los 599 pacientes que participaron en el estudio recibieron tromboprofilaxis con dosis baja de aspirina, heparina de bajo peso molecular o equivalente.
Conclusión Principal: Con una mediana de 6.8 meses de seguimiento y una mediana de cuatro ciclos recibidos, la SLP media y SG fue de 4.2 meses y 11.9 meses, respectivamente. La tasa global de respuesta fue del 35%, de los cuales, al menos un 8% de los pacientes obtuvo una respuesta parcial muy buena (RPMB). La mediana de duración de respuesta fue de 6.8 meses. Los pacientes refractarios al tratamiento previo con lenalidomida (n=572) o lenalidomida y bortezomib (n=473), alcanzaron una SLP similar (4.2 y 4.1 meses), una SG de 12 meses para cada uno y una tasa global de respuesta de entre el 34% y 35%.
Otros datos:
- Se realizó un análisis de subgrupos para determinar el impacto de la terapia en pacientes con insuficiencia renal moderada IRM). De los 604 pacientes que participaron en este análisis, 215 padecían una deficiencia renal moderada (aclaramiento de creatinina (DC) mayor de 45ml/min pero menor que 60ml/ min).
- La tasa global de respuesta fue similar entre los grupos de pacientes que recibieron pomalidomida más dosis bajas de dexametasona (37% con deficiencia renal moderada vs. 33% con deficiencia renal moderada) a pesar de las diferencias en la función renal.
- La duración de la respuesta media fue de 6 meses vs. 7.9 meses, respectivamente. La SLP fue mayor en pacientes sin deficiencia renal moderada, pero no alcanzó cifras significativas (3.7 vs. 4.6 meses, p= 0.1142).




