Introducción
La fabricación de máquinas que imitan al ser humano se ha mantenido por más de 4.000 años. Desde la aparición de autómatas y el amplio desarrollo industrial en el siglo XIX, las máquinas han ido evolucionando ampliamente hasta llegar a su máxima expresión coincidiendo con el desarrollo en mecánica, electrónica e informática1.
Dr. Joan Palou
Fuente: Fundación Puigvert / Mapa Media
Fue en 1920 cuando Karel Capek acuñó el término robot; vocablo checo que significa trabajo entendido como servidumbre, trabajo forzado.
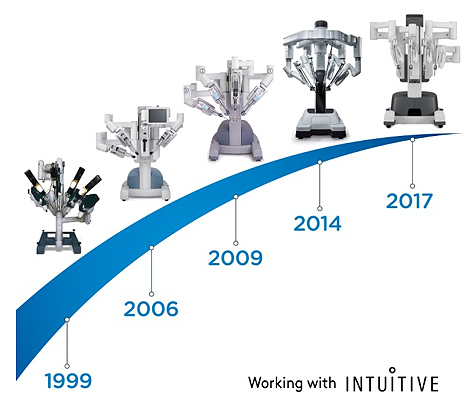
Figura 1
Fuente: Fundación Puigvert / Mapa Media
Primero surge la robótica industrial, con la automatización de procesos, hasta llegar a las primeras máquinas quirúrgicas en 1985 con el robot PUMA 560, utilizado para introducir una aguja en el cerebro en un TAC guiado2.
En la Fundació Puigvert utilizamos, durante años, un brazo robotizado, AESOP, para llevar a cabo las cirugías laparoscópicas. Se trataba de un brazo inteligente que reconocía la voz del cirujano y manipulaba la cámara según las órdenes recibidas.
En 1995 se constituyó la empresa Intuitive Surgical Inc en California, que llevó a cabo el diseño final del sistema ROBOT da Vinci. En realidad, se trata de un COBOT, ya que es un tipo de robot que asiste y facilita el trabajo pero no decide ni toma decisiones. El cirujano es el que dirige y realiza los movimientos de los brazos robóticos. Este ingenio requiere una elevada experticidad y conocimiento de la anatomía por parte del urólogo que lo manipula.
El sistema Robot da Vinci, que obtuvo la validación por la FDA en el año 2000, ha llegado hasta nuestros días con la evolución y mejora de sus modelos (Figura 1).
La primera cirugía robótica en España fue realizada en la Fundació Puigvert en el año 2005 para tratar a un paciente con cáncer de próstata. Desde entonces hemos sido pioneros en todos los ámbitos, incorporando este recurso en nuestro centro para la cirugía pediátrica, cirugía oncológica (cistoprostatectomía radical, nefrectomía parcial, nefrouretrectomía, etc...) y cirugía reconstructiva, hasta llegar a su implementación en el trasplante renal robótico3-6.
Ventajas del sistema robótico
La cirugía robótica incorpora, globalmente, las ventajas de la cirugía laparoscópica con la utilización de pequeñas incisiones cutáneas, menor dolor postoperatorio, mejor recuperación postoperatoria, menor estancia hospitalaria y menor transfusión sanguínea. Además, facilita el trabajo al cirujano, ya que se trabaja a diez aumentos, en 3D y no transmite el temblor de las manos. Todo ello redunda en una mejor técnica quirúrgica, hecho que aporta mayor beneficio para el paciente.
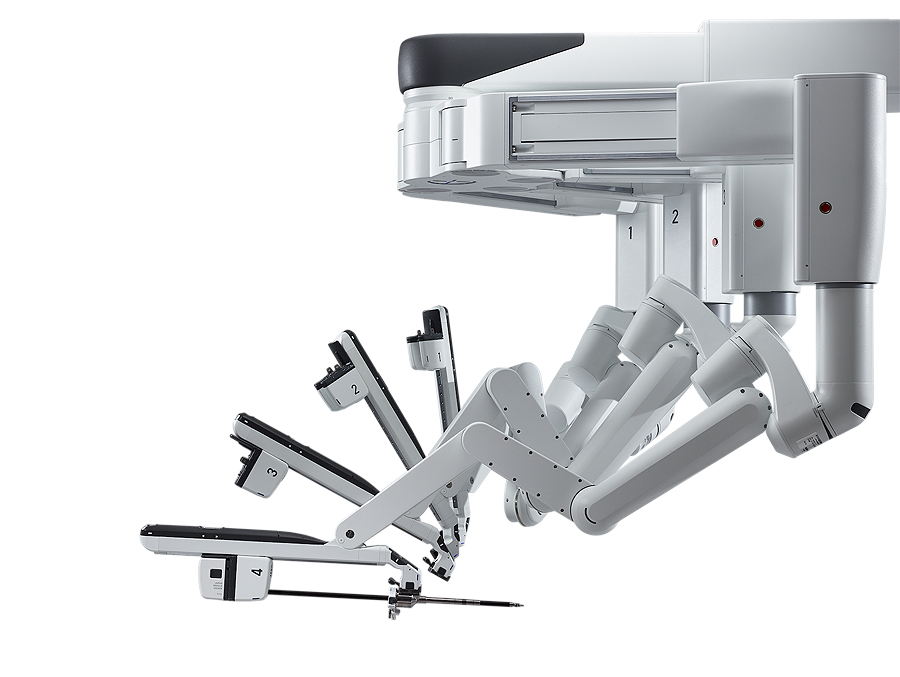
Detalle del robot Da Vinci
Fuente: Fundación Puigvert / Mapa Media
Aparte de que la cirugía robótica -como se ha comentado- facilita el trabajo al cirujano, también le proporciona confort, dado que se trabaja en una posición más ergonómica y cómoda, hecho que evita posiciones forzadas y daño muscular o tendinoso.
¿En qué consiste el sistema robótico?
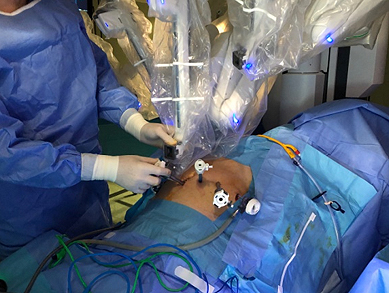
Figura 2
Fuente: Fundación Puigvert / Mapa Media
Se halla constituido por tres componentes: la consola, el sistema quirúrgico y el sistema de video. El cirujano está sentado ergonómicamente en la consola, apartado de la mesa quirúrgica. Desde el dispositivo avanzado, el cirujano activa y controla el corte, la coagulación, la posición de la cámara y el soporte del 4º brazo ayudante. El sistema quirúrgico consta de 3 o 4 brazos, uno de ellos para la óptica, otro para la tijera de corte, otro para la coagulación y el cuarto para colocar una pinza que actúa de ayudante. Además, podemos intercambiar y colocar instrumentos para sutura, etc. El sistema de video ofrece una imagen en 3D a través de una lente binocular que ofrece una imagen tridimensional perfecta para el cirujano.
Todos estos instrumentos entran a través de pequeñas incisiones por donde pasan los instrumentos que manipula el cirujano y el ayudante (Figura 2).
Evolución de la robótica en Medicina
Actualmente se han añadido nuevos robots que estarán pronto en el mercado. Los nuevos ingenios han sido desarrollados por diferentes casas comerciales (Transenterix, Cambridge Medical Robot, Medtronic, J and J, Distal Motion, Avatera, Medicaroid y otros).
Todo ello conllevará una mejora global y el perfeccionamiento de estos recursos.
El cirujano del futuro no sólo deberá conocer la anatomía y la enfermedad, sino también la tecnología, y deberá ser capaz de entenderla y manejarla.
Actualmente ya se practica con simuladores, hecho que facilita el paso de la teoría de la escuela de aprendizaje a la vida real en el paciente. El urólogo del siglo XXI debe aprender como los pilotos de aviación, y no con el paciente.

Detalle del robot Da Vinci
Fuente: Fundación Puigvert / Mapa Media
Bibliografía
1. Sánchez Martín FM, Millán Rodríguez F, Salvador Bayarri J, Palou Redorta J, Rodríguez Escovar F, Esquena Fernández S, Villavicencio Mavrich H. History of robotics: from Archytas of Tarentum until da Vinci robot. (Part I). Actas Urol Esp. 2007;31(2):69-76.
2. Sánchez-Martín FM, Jiménez Schlegl P, Millán Rodríguez F, Salvador-Bayarri J, Monllau Font V, Palou Redorta J, Villavicencio Mavrich H. History of robotics: from archytas of tarentum until Da Vinci robot. (Part II). Actas Urol Esp. 2007;31(3):185-96.
3. Villavicencio H. Technology of future: Da Vinci robotic surgery. Actas Urol Esp 2005;29(10):919-21.
4. Palou Redorta J, Gaya Sopena JM, Gausa Gascón L, Sánchez-Martín F, Rosales Bordes A, Rodríguez Faba O, Villavicencio Mavrich H. Robotic radical cystoprostatectomy: oncological and functional analysis. Actas Urol Esp. 2009;33(7):759-66.
5. Breda A, Territo A, Gausa L, Rodríguez-Faba O, Caffaratti J, de León JP, Guirado L, Facundo C, Guazzieri M, Guttilla A, Villavicencio H. Robotic kidney transplantation: one year after the beginning. World J Urol. 2017;35(10):1507-1515.
6. Hellenthal NJ, Hussain A, Andrews PE, Carpentier P, Castle E, Dasgupta P, Kaouk J, Khan S, Kibel A, Kim H, Manoharan M, Menon M, Mottrie A, Ornstein D, Palou J, Peabody J, Pruthi R, Richstone L, Schanne F, Stricker H, Thomas R, Wiklund P, Wilding G, Guru KA Surgical margin status after robot assisted radical cystectomy: results from the International Robotic Cystectomy Consortium. .J Urol. 2010;184(1):87-91.




