Prof.ª Mª José Alonso
A principios del siglo XX, el microbiólogo ruso y premio Nobel Iliá Ilich Méchnikov, estudiando los procesos de envejecimiento humano, observó que la población de ciertas poblaciones rurales de Europa, que se alimentaban principalmente de leche fermentada por bacterias ácido-lácticas, tenían una vida mucho más larga que otras poblaciones. Estas observaciones pueden considerarse el inicio de largas investigaciones que han llevado al complejo estudio del microbioma humano, es decir, el conjunto de microbios que lo habitan y su material genético, de la microbiota, que es la población específica de microbios que pueblan distintas cavidades y tejidos humanos, y de los probióticos, definidos en 2002 por la FAO y la Organización Mundial de la Salud como aquellos “microorganismos vivos que cuando se administran en las cantidades adecuadas confieren un beneficio para la salud del huésped”[1].

Prof.ª Mª José Alonso
Fuente: Prof.ª Alonso
El microbioma humano puebla la piel, orofaringe, tracto gastrointestinal, tracto genitourinario y tejido mamario entre otros, aunque la mayor concentración de microbios se localiza en el intestino y cumple en el organismo importantes funciones: nutricionales y metabólicas (a nivel intestinal producen energía y ayudan a la producción y absorción de vitaminas y minerales y a hidrolizar nutrientes que de otra forma no podrían ser asimilados), de protección (previenen la invasión de otros gérmenes o el sobrecrecimiento de microorganismos patógenos) y juegan un importante papel en el desarrollo del sistema inmunitario.
Actualmente se sabe que los sistemas ecológicos microbianos son similares en zonas anatómicas específicas que son comunes a diferentes personas; no obstante, variará de una persona a otra en las distintas cavidades y tejidos en función de la alimentación, el modo de vida (higiene, comportamiento social…) y la genética.
La microbiota puede también ser diferente para una misma persona en diferentes momentos de la vida en las mismas zonas anatómicas debido a cambios en la dieta, tratamientos farmacológicos o cambios en el medio ambiente.
Ciertas enfermedades (patologías intestinales, alergias, problemas inmunitarios, asma, trastornos de la piel, candidiasis y afecciones bucodentales entre otras) se han relacionado con alteraciones de la microbiota (disbiosis), aunque en algunos casos no se sabe a ciencia cierta si la alteración de la microbiota es la causa de la enfermedad o si es la enfermedad la que altera el equilibrio de la microbiota.
De los resultados de todos estos estudios se desprende que la administración de probióticos estaría indicada para prevenir y restablecer el equilibrio de la microbiota; por lo tanto, sería recomendable cuando se presentan situaciones en que la microbiota sufre alteraciones o riesgo de ser alterada y en aquellas situaciones en que se presentan síntomas relacionables con una disbiosis.
En la actualidad se están llevando a cabo importantes estudios sobre el papel beneficioso que los probióticos pueden jugar durante el embarazo, la lactancia y la infancia en relación con la prevención de complicaciones en el parto, un buen desarrollo inmunitario del niño y el adulto y la prevención de enfermedades atópicas, entre otros beneficios.
Cabe destacar, no obstante, que no todos los probióticos sirven para todo. Distintas cepas probióticas y distintas combinaciones han demostrado su eficacia para equilibrar la microbiota en distintas cavidades, tejidos y/o situaciones, por lo que en la administración de probióticos, debe tenerse en cuenta qué cepa o combinación de cepas bacterianas beneficiosas son las más convenientes para el beneficio que se quiere obtener.
Probióticos en la etapa preconceptiva, el embarazo y la lactancia
La amplia investigación realizada en los últimos años sobre la microbiota ha puesto de manifiesto su importancia tanto en la salud reproductiva como en la repercusión que una buena o mala microbiota puede tener sobre la salud del niño (y del adulto en que se convertirá) desde la gestación, durante la lactancia y en las primeras etapas de la vida.
Etapa preconceptiva
Los lactobacilos mantienen en la vagina un ambiente ácido que la defiende de distintas infecciones y ejercen además una función ‘barrera’ al evitar la adhesión a las células epiteliales vaginales de microbios que podría infectarlas; de esta manera ayudan a proteger la integridad de la superficie de la mucosa.
Una de las infecciones vaginales más frecuentes en las mujeres de edad fértil es la vaginosis bacteriana (VB). Se produce por una alteración de la microbiota vaginal consistente en el reemplazo de los beneficiosos lactobacilos vaginales (principales constituyentes) por otras bacterias, sobre todo anaeróbicas, principalmente Gardnerella vaginalis, pero también Atopobium vaginae, Prevotella, Peptostreptococcus y Bacteroides.
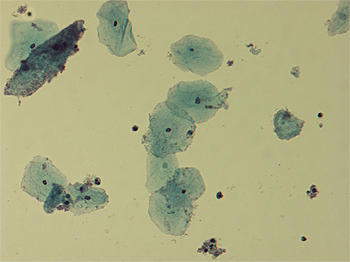
Vista microscópica de Gardnerella vaginalis
Autor/a de la imagen: Dr. F.C. Turner - Photographed myself using Olympus BX50 microscope on the Department of Pathology, University Medical Center Groningen, The Netherlands.
Fuente: Wikipedia
Se estima que la vaginosis bacteriana (VB) tiene una prevalencia de aproximadamente el 19% en la población infértil. Estas observaciones sugieren que una microbiota vaginal anormal puede estar asociada a resultados reproductivos deficientes, dado además que la VB es a menudo subclínica y por tanto no tratada. Aunque se han realizado pocos estudios en mujeres infértiles, los resultados de los realizados han sugerido que la presencia de VB tiene un impacto negativo en la fecundidad. Los microorganismos responsables impactan negativamente sobre el esperma y sobre la implantación del embrión. Un reciente estudio en una cohorte de 130 pacientes infértiles que asistían al tratamiento de fertilización in vitro (FIV) (Haahr, T. 2016)[2] dio como resultado que el 21% de las pacientes tenían una VB con altas concentraciones de G. vaginalis y / o A. vaginae. La tasa general de embarazo clínico fue del 35% (29/84). Curiosamente, solo el 9% (2/22) con una microbiota vaginal anormal obtuvo un embarazo clínico (P = 0,004).
Los autores concluyeron que sería beneficioso que las pacientes se sometiesen a un examen de detección de VB y, en caso necesario, posterior tratamiento probiótico para normalizar la microbiota vaginal anormal antes de someterse a un tratamiento de fertilidad. Esto hace pensar asimismo que el mismo protocolo sería conveniente cuando una mujer en edad fértil decide quedar embarazada.
Embarazo: Parto prematuro y preeclampsia
Asimismo, durante el embarazo la vaginosis bacteriana aumenta el riesgo de parto prematuro hasta en un 40% (Hillier et al.). Lactobacillus representa la especie dominante en la vagina de la mayoría de las mujeres embarazadas sanas. Se ha sugerido la administración oral o vaginal de Lactobacillus para prevenir la vaginosis bacteriana y posiblemente reducir el riesgo de parto prematuro (Yang et al 2015; Hillier et al 1999)[3,4].
En cuanto a la preeclampsia, se ha sugerido que los probióticos pueden modificar la inflamación del trofoblasto placentario, la inflamación sistémica y la presión arterial, aspectos relacionados con el desarrollo de preeclampsia. Un estudio de cohorte realizado en madres e hijos noruegos en 33.399 mujeres primíparas en los años 2002-2008, asoció el consumo regular de probióticos lácticos en el embarazo con un menor riesgo de preeclampsia en mujeres primíparas (Bransaeter et al 2011)[5].
Importancia de la transferencia de bacterias de la madre al niño
Hasta hace relativamente pocos años se pensaba que la colonización gastrointestinal del niño comenzaba en el canal del parto a partir de la cavidad oral, y que en la etapa fetal el intestino del feto era estéril.
No obstante, estudios más recientes han demostrado que, aunque la colonización masiva ocurre durante el parto y continúa durante la lactancia, el desarrollo de la microbiota intestinal se inicia en la vida intrauterina a través de la placenta y el líquido amniótico. En la actualidad está científicamente aceptado que la exposición a los microorganismos maternos durante la gestación depende del estado nutricional, metabólico e inmunológico de la madre (De la Rosa et al. 2014)[6].
Las bacterias beneficiosas transferidas al niño desde la madre pueden equilibrar la respuesta inmune, suprimir la hipersensibilidad y reducir las reacciones alérgicas y el eczema. (Mortensen et al 2016)[7]. También se ha relacionado con una reducción de los trastornos digestivos como el cólico del lactante y una reducción de la posibilidad de infecciones al fortalecer el sistema inmunitario.
Estudios basados en cultivos han demostrado que la colonización intestinal por Lactobacillus, Bifidobacterium y Bacteroides en bebés nacidos por cesárea se retrasa, y se sabe que la composición de la microbiota inicial puede tener implicaciones para las funciones nutricionales e inmunológicas asociadas con la microbiota en desarrollo.
Investigaciones recientes sugieren que los bebés nacidos por cesárea pueden ser más susceptibles a alergias y asma, y muestran que la administración de probióticos desde el nacimiento hasta los 6 meses de edad reducía la incidencia de alergia a los 5 años en niños nacidos por cesárea (Dominguez-Bello et al 2010)[8].
La colonización inicial es importantísima, ya que sienta las bases para el microbioma adulto relativamente estable de por vida (Turnbaugh et al. 2009; Martínez et al 2018)[9,10].
Probióticos en la infancia
Diversas investigaciones apuntan a que una suplementación temprana de probióticos podría reducir el impacto del cólico del lactante y reducir el riesgo de desarrollo de respuestas autoinmunes, alergias y eczemas.
Cólico del lactante
El cólico del lactante es uno de los problemas más comunes en los primeros tres meses de vida y afecta a entre el 10% y el 30% de los niños recién nacidos. La causa exacta del cólico es desconocida, y se revela como multifactorial: un sistema digestivo inmaduro, la producción excesiva de gas y el trastorno digestivo son las causas más asociadas al cólico.
Las investigaciones realizadas muestran que en los bebés con cólico del lactante se han observado recuentos más bajos de lactobacilos intestinales que en los bebés que no los sufren (Savino F. et al 2005)[11]. Diversos estudios muestran que la ingesta diaria de L. Reuteri solo y en combinación con L. Rhamnosus puede acortar la duración del llanto y la molestia en los bebés con cólicos. (Meneghin t al 2013; Garassimov et al 2018)[12,13].
Se cree que la malabsorción de lactosa es una de las principales causas de los cólicos, afectando del 10% al 20% de los recién nacidos. Cuando la lactosa no se descompone en el intestino delgado, puede causar gas en el intestino grueso, que puede ser la causa del dolor. Se sabe que los lactobacilos también producen lactasa, que es la enzima necesaria para convertir la lactosa de la leche materna en glucosa y galactosa. Un reciente ensayo controlado con placebo en 168 bebés mostró que una combinación de L. Reuteri y L Rhamnosus con vitamina D3 vs vitamina D3 sola, tuvo un efecto significativamente mayor en la reducción de los cólicos. Una de las hipótesis barajadas es que su efecto se deba a que la flora intestinal de los niños con cólicos no está completamente desarrollada y que tienen dificultades para descomponer la lactosa en el intestino delgado, y la suplementación aumenta la producción de lactasa[14].
Reducción del riesgo de autoinmunidad
Un importante estudio de cohorte estadounidense con 8.676 niños mostró que la suplementación temprana con probióticos (a la edad de 0-27 días) se asocia con una disminución significativa (3%) del riesgo de autoinmunidad. Por lo tanto, los probióticos podrían, en teoría, prevenir la diabetes tipo 1, y enfermedades autoinmunes como esclerosis, artritis, etc., en su futuro de vida. (Uusitalo et al 2016[15].
Alergia y eczema
Se estima que un 15-20% de los niños en el mundo occidental tienen dermatitis atópica (DA) y que hasta la mitad de los que tienen eccema infantil desarrollarán asma más adelante durante la vida (American Academy of Allergy Asthma & Immunology). Hasta el 40% de los niños con DA moderada a severa también tienen algún tipo de alergia alimentaria, aunque no está claro si los alimentos pueden causar DA.
No se conocen las causas de la dermatitis atópica, pero parece estar muy involucrado el deterioro de la barrera mucosa y la disbiosis. La barrera dañada puede conducir a la migración de antígenos alimentarios al torrente sanguíneo, lo que puede comprometer el equilibrio del sistema inmunológico.
Algunos estudios también indican que los pacientes con DA tienen un sistema inmunitario desequilibrado con una respuesta Th-2 predominante (Hamid et al. 1994)[16]. Según la ‘hipótesis de la higiene’, la incidencia decreciente de infecciones en los países occidentales conduce a una incidencia cada vez mayor tanto de enfermedades autoinmunes como alérgicas. Cuando no estamos expuestos a antígenos dañinos, el sistema inmunológico se vuelve perezoso y comienza a reaccionar contra antígenos inofensivos como las proteínas de la leche, etc.
Estudios realizados en hospitales daneses muestran que la suplementación con una combinación de Lactobacillus reuteri y L Rhamnosus puede estabilizar la función de barrera y reducir la alergia y el eccema infantil (Rosenfeldt et al 2003 y Rosenfeldt el al 2004)[17,18].
Infección por rotavirus
Otro de los problemas frecuentes que afectan a los niños durante el primer año de vida son las infecciones por rotavirus, causantes del 70% de casos de diarrea en lactantes y niños. Las infecciones por rotavirus pueden afectar de distinta manera a los niños, de forma que en algunos desaparecerá en pocos días con cambios alimenticios y rehidratación, mientras que en otros el cuadro se manifiesta de forma más severa con abundante diarrea y vómitos y riesgo de deshidratación, por lo que pueden requerir incluso hospitalización.
Estudios realizados en Dinamarca han demostrado que una combinación de L. Reuteri y L. Rhamnosus reduce significativamente la diarrea inducida por el virus (tanto en pacientes hospitalizados como no hospitalizados). El beneficio se relaciona con la capacidad de estos probióticos para colonizar la mucosa intestinal y prevenir la infección viral en las células epiteliales (Rosenfeldt el al 2002a; Rosenfeldt et al 2002b)[19,20].
Un reciente metaanálisis (Ahmadi et al 2015)[21] ha concluido que ciertos probióticos (como L. Reuteri, combinaciones de L. Reuteri y L. Rhamnosus y Saccharomyces boulardii) ejercen un efecto positivo en la reducción de la duración de la diarrea aguda causada por rotavirus comparado con el control.
Otro de los efectos positivos de los probióticos, demostrado en múltiples estudios, es la prevención y reducción de síntomas de diarrea en pacientes en tratamiento con antibiótico. La diarrea por antibióticos, según se estima, afecta al 20% de los pacientes tratados con estos medicamentos. (Blaabjerg et al 2017)[22]. El uso de probióticos junto con los antibióticos puede ayudar además a prevenir el sobrecrecimiento de especies patógenas oportunistas resistentes a los antibióticos.
La combinación beneficiosa de B. Lactis, L. Reuteri y L. Rhamnosus con DHA y EPA
En cuanto a la combinación de bacterias beneficiosas como Bifidobacterium lactis (32269), Lactobacillus reuteri (12246) y Lactobacillus rhamnosus (19070-2) con ácidos omega 3 (DHA y EPA) para el embarazo y la lactancia, de entrada cabe destacar que EPA y DHA son componentes estructurales de nuestro organismo que intervienen en numerosos procesos biológicos. El DHA es un componente esencial para el desarrollo del cerebro y la retina del feto. Estos ácidos grasos omega 3 se deben ingerir a través de la dieta o suplementos, ya que nuestro organismo no los sintetiza. Normalmente, por la dieta se obtienen a partir del pescado, pero durante el embarazo el consumo de pescado, tal como han advertido las autoridades sanitarias, se debe limitar debido al riesgo de efectos adversos por mercurio en el desarrollo del feto.

Un complemento alimenticio
Fuente: Cien por Cien Natural
Diversos estudios han demostrado que la suplementación con omega 3 durante el embarazo se asocia con un mejor desarrollo neurológico en el niño y además juega un papel importante en la prevención de la preeclampsia durante el embarazo, y de la depresión postparto. Por otra parte, los probióticos (lactobacilos y bifidobacterias) administrados por vía oral migran a la vagina y pueden prevenir la vaginosis bacteriana, afección que podría llevar a un parto prematuro; además, las bacterias beneficiosas se transfieren de la madre al niño a través del parto y pueden equilibrar la respuesta inmune del bebé y reducir la aparición de reacciones alérgicas como el eccema.
La dosis mínima diaria de DHA estipulada por las autoridades europeas (EFSA) para las embarazadas es de 200 mg DHA/día, y la dosis máxima de 450 mg. Estas dosis se estimaron a partir de los resultados de los diversos estudios que se han hecho en madres y bebés.
L. Rhamnosus y L. Reuteri pueblan los intestinos y la vagina y desempeñan un papel esencial para el funcionamiento digestivo e inmunológico, así como para prevenir la colonización de bacterias patógenas invasoras al adherirse a la pared intestinal y desplazar a las bacterias y levaduras hostiles. Durante un parto, un recién nacido recoge la microflora bacteriana vaginal de su madre a través del canal de parto. Cuando se realiza una cesárea, la microflora materna no se transfiere de madre a hijo y se ha demostrado que esta es la razón por la que algunos bebés nacidos por cesárea desarrollan alergias (incluida la dermatitis atópica), por lo que es conveniente suplementar con probióticos a estos niños. La otra forma muy importante de transferir la microflora materna de la madre al bebé es mediante la lactancia, por lo que se debe cuidar también -durante la lactancia- que la madre tenga una microbiota bien equilibrada.
Conclusiones
Los probióticos, especialmente los lactobacilos, juegan un importante papel en la salud de la embarazada y del niño. De los estudios realizados se puede concluir que:
▪ En el embarazo, la administración de probióticos puede reducir el riesgo de vaginosis bacteriana (ésta puede causar problemas de fertilidad y la aparición de parto prematuro).
▪ La transferencia de bacterias beneficiosas de la madre al niño durante el embarazo, el parto y la lactancia, puede equilibrar la respuesta inmune, suprimir la hipersensibilidad, y reducir las reacciones alérgicas y el eczema. Una microbiota saludable en la madre influye en la buena colonización del infante.
▪ La administración de probióticos se ha demostrado que puede reducir el cólico del lactante.
▪ La administración de probióticos puede reducir significativamente la diarrea por rotavirus y por uso de antibióticos.
Debe tenerse en cuenta, no obstante, que no todas las cepas probióticas sirven para todo y que en cada caso deberían utilizarse aquellas cepas que han demostrado mediante estudios la utilidad para los efectos que se buscan. Asimismo, el uso de probióticos no debe generalizarse y, aunque su perfil de seguridad es muy bueno, no se recomienda la ingesta de probióticos sin supervisión del especialista a pacientes con sistema inmune muy debilitado, a personas inmunocomprometidas o a personas con sangrado intestinal.
Referencias
1. Joint FAO/WHO Working Group Report on Drafting Guidelines for the Evaluation of Probiotics in Food London, Ontario, Canada, April 30 and May 1, 2002
2. Haahr T. Abnormal vaginal microbiota may be associated with poor reproductive outcomes: A prospective study in IVF patients. Journal of Reproductive Immunology, 115, 47-48. doi: 10.1016 / j.jri.2016.04.144
3. Yang S, Reid G, Challis JR, Kim SO, Gloor GB, Bocking AD. Is there a role for probiotics in the prevention of preterm birth? Front Immunol. 2015 Feb 17;6:62. doi: 10.3389/fimmu.2015.00062.
4. Hillier SL, Nugent RP, Eschenbach DA, Krohn MA, Gibbs RS, Martin DH, Cotch MF, Edelman R, Pastorek JG 2nd, Rao AV, McNellis D, Regan JA, Carey JC, Klebanoff MA, for the Vaginal Infections and Prematurity Study Group: Association between bacterial vaginosis and preterm delivery of a low-birth-weight infant. N Engl J Med 1995, 333(26):1737–1742.
5. Bransaeter et al. Intake of Probiotic Food and Risk of Preeclampsia in Primiparous Women: The Norwegian Mother and Child Cohort Study. American Journal of Epidemiology, 174(7), 807-815
6. De la Rosa D et al. La microbiota intestinal en el desarrollo del sistema inmune del recién nacido. Revista Cubana de Pediatría. 2014;86(4):502-513
7. Mortensen MS1, Brejnrod AD1, Roggenbuck M1, Abu Al-Soud W1, Balle C1, Krogfelt KA2, Stokholm J3, Thorsen J3, Waage J3, Rasmussen MA3,4, Bisgaard H3, Sørensen SJ5. The developing hypopharyngeal microbiota in early life. Microbiome. 2016 Dec 30;4(1):70. doi: 10.1186/s40168-016-0215-9.
8. Dominguez-Bello MG1, Costello EK, Contreras M, Magris M, Hidalgo G, Fierer N, Knight R. Delivery mode shapes the acquisition and structure of the initial microbiota across multiple body habitats in newborns. Proc Natl Acad Sci U S A. 2010 Jun 29;107(26):11971-5. doi: 10.1073/pnas.1002601107
9. Turnbaugh PJ, Hamady M, Yatsunenko T, et al. A core gut microbiome in obese and lean twins. Nature. 2008;457(7228):480-4.
10. Martínez et al. Experimental evaluation of the importance of colonization history in early-life gut microbiota assembly. eLife 2018;7:e36521 DOI: 10.7554/eLife.36521
11. Savino F, Bailo E, Oggero R, Tullio V, Roana J, et al. (2005) Bacterial counts of intestinal Lactobacillus species in infants with colic. Pediatr Allergy Immunol 16: 72-75.
12. Meneghin F, Dilillo D, Mantegazza C, Galli E, Stucchi S, et al. (2013) Live Probiotic Culture Supplementation in the Treatment of Infantile Colic: A Review of Literature. J Prob Health 1: 104. Doi: 10.4172/2329-8901.1000104
13. Garassimov et al. 2018.ClinicalTrials.gov Identificador: NCT02839239 https://clinicaltrials.gov/ct2/show/NCT02839239
14. Effect of Lactocare Baby Drops in Infants Colic, Clinical Trials.gov Identifier:NCT02839239 [study ongoing – not published yet]
15. Uusitalo et al. Association of Early Exposure of Probiotics and Islet Autoimmunity in the TEDDY Study. JAMA Pediatr. 2016 Jan;170(1):20-8. doi: 10.1001/jamapediatrics.2015.2757
16. Hamid el al. Differential in situ cytokine gene expression in acute versus chronic atopic dermatitis. J Clin Invest. 1994 Aug;94(2):870-6.
17. Rosenfeldt et al . Effect of probiotic Lactobacillus strains in children with atopic dermatitis. J Allergy Clin Immunol. 2003 Feb;111(2):389-95.
18. Rosenfeldt et al. Effect of probiotics on gastrointestinal symptoms and small intestinal permeability in children with atopic dermatitis. J Pediatr 2004;145:612-6
19. Rosenfeldt et al. (a) Effect of probiotic Lactobacillus strains in young children hospitalized with acute diarrhea Pediatr Infect Dis J, 2002;21:411–16
20. Rosenfeldt et al. (b) Effect of probiotic Lactobacillus strains on acute diarrhea in a cohort of nonhospitalized children attending day-care centers
21. Ahmadi E, Alizadeh-Navaei R, Rezai MS. Efficacy of probiotic use in acute rotavirus diarrhea in children: A systematic review and meta-analysis. Caspian J Intern Med. 2015;6(4):187-95.
22. Blaabjerg S, Artzi DM, Aabenhus R. Probiotics for the Prevention of Antibiotic-Associated Diarrhea in Outpatients-A Systematic Review and Meta-Analysis. Antibiotics (Basel). 2017;6(4):21. Published 2017 Oct 12. doi:10.3390/antibiotics6040021