Redacción Farmacosalud.com
La combinación de una triple terapia a base de encorafenib, binimetinib y cetuximab aumenta en un 70% la supervivencia global (SG) madura en cáncer colorrectal metastásico BRAFV600E, en tanto que la mediana de SG madura registrada es de 15,3 meses, lo que contrasta con la media de 9 meses registrada con otros tratamientos para este tumor, que se caracteriza por su mal pronóstico. La SG madura significa que existe un mayor número de pacientes analizados y un mayor tiempo de seguimiento, por lo que los datos son más robustos y concluyentes.

Fuente: www.farmacosalud.com
La compañía Pierre Fabre ha anunciado los resultados actualizados de seguridad y eficacia, incluyendo datos maduros de supervivencia global, del grupo inicial de seguridad del estudio de fase III BEACON CRC que evaluaba la triple combinación de BRAFTOVI® (encorafenib), un inhibidor de BRAF, MEKTOVI® (binimetinib), un inhibidor de MEK, y ERBITUX® (cetuximab), un anticuerpo monoclonal anti-EGFR, en pacientes con cáncer colorrectal metastásico (CCRm) con la mutación de BRAFV600E. Los resultados muestran que la mediana de SG madura es de 15,3 meses (IC 95%; 9,6–No alcanzado) para los pacientes tratados con la triple combinación.
“El cáncer colorrectal BRAF mutado es un tumor de particular mal pronóstico. Se estima que la supervivencia de estos pacientes se encuentra en torno a los 9 meses. Sin embargo, la incorporación de regímenes de tratamiento más intenso, y sobre todo, el hecho de conocer mejor la biología de estos tipos de tumores junto con el diseño de fármacos dirigidos como este régimen de tratamiento, han permitido cambiar estas estadísticas”, afirma a través de www.farmacosalud.com la Dra. Elena Élez, especialista en oncología médica del Hospital Vall d'Hebron -particularmente en cáncer colorrectal-, investigadora clínica del VHIO (Vall d'Hebron Institute of Oncology-Vall d’Hebron Instituto de Oncología) [Barcelona] y una de las firmantes del estudio.
La mutación de BRAF, presente en hasta un 15% de los pacientes con CCRm
Los resultados de la mediana de supervivencia libre de progresión (mSLP) y la tasa de repuesta global (TRG) actualizados para los pacientes tratados con la triple combinación en el grupo inicial de seguridad se mantienen igual a los previamente comunicados, con 8 meses de mSLP (IC 95%; 5,6–9,3) y un 48% de TRG (IC 95%; 29,4–67,5). En los 17 pacientes que recibieron solamente una línea de tratamiento previa, la TRG fue del 62%.

Dr. Josep Tabernero
Fuente: Hospital Universitario Vall d'Hebron / ARCHIVO
“Estamos encantados viendo unos datos alentadores como los del estudio BEACON CRC, en los que una SG Madura de 15,3 meses representa una mejora remarcable en comparación con los estándares de tratamiento para los pacientes con CCRm BRAF mutado”, remarca el Dr. Josep Tabernero, MD, PhD, investigador del estudio BEACON CRC y director del Instituto de Oncología Vall d’Hebron de Barcelona. “Estos últimos datos nos acercan aún más a la comprensión de todo el potencial que puede tener esta triple terapia como una posible nueva opción de tratamiento para estos pacientes”, añade.
La mutación de BRAF está presente en hasta un 15% de los pacientes con CCRm; la V600E es la mutación más frecuente de BRAF[1-5]. Las personas que padecen CCRm con la mutación BRAFV600E tienen un riesgo de mortalidad superior al doble del que tienen aquellos pacientes con un CCRm sin la mutación. Actualmente, en los casos con mutación no existen tratamientos aprobados por la Comisión Europea (CE) específicamente dirigidos a esta población con una gran necesidad no cubierta[3-10].
Según la Dra. Élez, para estos enfermos existen hoy en día varias estrategias terapéuticas: “Dado que esta mutación tiene implicaciones pronósticas, solemos aconsejar tratamientos intensos en la primera línea que incluyen dos o tres quimioterápicos (según las condiciones físicas del paciente) y la asociación del anticuerpo antiangiogénico bevacicumab. En segunda línea de tratamiento, una vez se constata progresión de la enfermedad al primer esquema iniciado, solemos emplear combinaciones de dos quimioterápicos y también algún anticuerpo antiangiogénico como bevacizumab o aflibercept. En este último caso, se ha demostrado particular beneficio para la población BRAF mutada”.
Buen perfil de seguridad
Para la Dra. Élez, otra de las grandes virtudes de la triple combinación a base de encorafenib, binimetinib y cetuximab es que, en la mayoría de los casos, los efectos adversos observados suelen ser leves: “Esta es una de las principales ventajas del tratamiento, puesto que no estamos hablando de quimioterapia, sino de terapia dirigida. Normalmente, aquellos pacientes que presentan algún tipo de efecto secundario (suele ser una erupción en la piel) suelen presentar eventos adversos leves y reversibles, y raramente se requiere suspender o retrasar el tratamiento por los mismos”.

Dra. Elena Élez
Fuente: Despacho Dra. Élez / VHIO
Los efectos adversos más comunes de grado 3 o 4 observados en al menos un 10% de los pacientes fueron la fatiga (13%), la anemia (10%), el incremento de la creatinina fosfoquinasa (10%), el incremento del aspartato aminotransferasa (10%) y las infecciones del tracto urinario (10%). La tasa de toxicidades cutáneas de grado 3 o 4 continuó siendo más baja que la generalmente observada en el tratamiento con ERBITUX en el CCRm.
“Los alentadores resultados actualizados de la SG del grupo inicial de seguridad del estudio BEACON CRC demuestran el potencial terapéutico de la triple combinación de BRAFTOVI, MEKTOVI y ERBITUX para el tratamiento de los pacientes con un CCRm con mutación de BRAFV600E, un cáncer notoriamente difícil de tratar,” subraya Frédéric Duchesne, presidente & CEO de la División Farmacéutica de Pierre Fabre. “Estos recientes resultados nos complacen enormemente, pues van en consonancia con nuestra estrategia de I+D orientada a aquellos tumores en los que los pacientes tienen una mayor necesidad, enfatizando en los tratamientos dirigidos a biomarcadores”, agrega Duchesne.
Cáncer colorrectal: el tercer cáncer más frecuente en hombres y el segundo en mujeres
El 20 de septiembre de 2018, la CE garantizó la autorización de comercialización de la combinación de BRAFTOVI y MEKTOVI para el tratamiento de los pacientes adultos con melanoma no resecable o metastásico con la mutación de BRAFV600 detectada por un test validado[11,12]. La decisión de la CE implica a todos los 28 Estados miembros de la Unión Europea, además de Liechtenstein, Islandia y Noruega.
El 7 de agosto de 2018, La Administración de Alimentos y Fármacos de los Estados Unidos (FDA, por sus siglas en inglés) garantizó la designación como Terapia Innovadora de BRAFTOVI, en combinación con MEKTOVI y ERBITUX, para el tratamiento de los pacientes con CCRM con la mutación BRAFV600E detectada por un test aprobado por la FDA, tras el fracaso a uno o dos líneas de tratamiento previo para la enfermedad metastásica[13]. La triple combinación de BRAFTOVI, MEKTOVI y ERBITUX para el tratamiento de los pacientes con CCRm con la mutación de BRAFV600E está en fase de investigación y aún no ha sido aprobada por la CE.
TAC relativo al cáncer colorrectal
Fuente: Archivo
En todo el mundo, el cáncer colorrectal supone el tercer tipo de cáncer más frecuente en hombres y el segundo más frecuente en mujeres, con aproximadamente 1,4 millones de nuevos casos diagnosticados en 2012. Globalmente en 2012, aproximadamente 694.000 muertes se atribuyeron al cáncer colorrectal[14]. Solo en EE.UU. se estimaba que 140.250 pacientes serían diagnosticados de cáncer de colon o recto durante 2018, y que aproximadamente 50.000 morirían por la enfermedad[15].
Sobre el BEACON CRC
El estudio BEACON CRC es un estudio aleatorizado, abierto y global que evalúa la eficacia y seguridad de BRAFTOVI, MEKTOVI y ERBITUX en pacientes con CCRm con la mutación BRAFV600E que han progresado a una o dos líneas de tratamiento previas. El BEACON CRC es el primer estudio de fase III diseñado para testar una combinación de tratamiento dirigida a BRAF y MEK en CCRm con la mutación BRAFV600E. Treinta pacientes fueron tratados en un grupo inicial de seguridad y recibieron la triple combinación (BRAFTOVI 300 mg diarios, MEKTOVI 45 mg dos veces al día y ERBITUX según indicación). De los 30 pacientes, 29 tenían la mutación de BRAFV600.
La inestabilidad de microsatélites elevada (MSI-H, por sus siglas en inglés), resultado de un defecto de reparación de desajustes en el ADN, se detectó en solamente 1 de los pacientes. Como previamente ya se había anunciado, la triple combinación había demostrado un buen perfil de tolerabilidad, que apoyó el inicio de la parte aleatorizada del estudio. La parte aleatorizada del estudio BEACON CRC se diseñó para evaluar la eficacia de BRAFTOVI en combinación con ERBITUX con o sin MEKTOVI en comparación con ERBITUX y un tratamiento basado en irinotecán. Se esperaba incluir aproximadamente 615 pacientes aleatorizados 1:1:1 a recibir la triple combinación, la doble combinación (BRAFTOVI y ERBITUX) o el tratamiento del brazo control (un tratamiento basado en irinotecán y ERBITUX). El estudio ha sido enmendado para incluir un análisis interino de los objetivos, incluyendo la TRG. El objetivo principal de la supervivencia global es una comparación de la triple combinación con el brazo control.
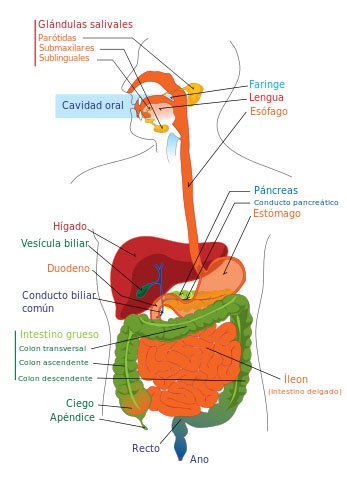
Autor/a: Mariana Ruiz (English version); User:Bibi Saint-Pol, Jmarchn (Spanish version, translation by User:AlvaroRG) - Own work; translated from Image:Digestive system diagram en.svg
Fuente: Wikipedia
Los objetivos secundarios se dirigen a evaluar la eficacia de la doble combinación en comparación con el brazo control y de la triple combinación en comparación con la doble combinación. Otros objetivos secundarios incluyen la SLP, la duración de la respuesta, la seguridad y la tolerabilidad. También se evalúan datos de calidad de vida relacionados con la salud. El estudio se está realizando en más de 200 centros de investigación en Norte América, Sudamérica, Europa y la región de Asia-Pacífico. El reclutamiento del estudio se completó en 2018. El trabajo BEACON CRC se está realizando con el soporte de Ono Pharmaceutical Co., Pierre Fabre y Merck KGaA, Darmstadt, Alemania (este soporte es para los centros de fuera de Norteamérica).
Sobre BRAFTOVI (encorafenib) y MEKTOVI (binimetinib)
BRAFTOVI (encorafenib) es una molécula pequeña oral que inhibe la quinasa BRAF, mientras que MEKTOVI (binimetinib) es una molécula pequeña oral que inhibe MEK; ambas se ligan a enzimas clave de la vía de señalización de las MAP quinasas (MAPK, por sus siglas en inglés) (RAS-RAF-MEK-ERK).
La activación inapropiada de las proteínas de la vía ha demostrado que puede aparecer en muchos cánceres, incluyendo el melanoma, el cáncer colorrectal, el cáncer de pulmón no célula pequeña y otros. En Europa, la combinación está aprobada para el tratamiento de los pacientes adultos con un melanoma no resecable o metastásico con la mutación BRAFV600, detectada por un test validado.
Referencias
1. Sorbye H, et al. PLoS One. 2015;10(6):e0131046.
2. Vecchione L, et al. Cell. 2016;165(2):317–330.
3. Saridaki Z, et al. PLoS One. 2013;8(12):e84604.
4. Loupakis F, et al. Br J Cancer. 2009;101(4):715–721.
5. Corcoran RB, et al. Cancer Discov. 2012;2(3):227–235.
6. Kopetz et al. J Clin Onc.2017;35(15):3505-3505.
7. De Roock W, et al. Lancet Oncol. 2010;11(8):753–762.
8. Ulivi P, et al. J Transl Med. 2012;10:87.
9. Peeters et al. J Clin Onc.2014; 32(15):3568-3568.
10. Ardekani R, et al. PLoS One. 2012;7(7):e40506.
11. European Medicines Agency. BRAFTOVI® Summary of Product Characteristics, November 2018. Available at: https://www.ema.europa.eu/documents/product-information/braftovi-epar-product-information_en.pdf. Accessed January 2019.
12. European Medicines Agency. MEKTOVI® Summary of Product Characteristics, November 2018. Available at: https://www.ema.europa.eu/documents/product-information/mektovi-epar-product-information_en.pdf. Accessed January 2019.
13. Array BioPharma. Array Biopharma Receives FDA Breakthrough Therapy Designation For Braftovi™ In Combination With Mektovi® And Cetuximab For BRAFV600E-Mutant Metastatic Colorectal Cancer. Available at: http://investor.arraybiopharma.com/news-releases/news-release-details/array-biopharma-receives-fda-breakthrough-therapy-designation. Accessed January 2019.
14. Global Cancer Facts & Figures 3rd Edition. American Cancer Society. Available at: https://www.cancer.org/content/dam/cancer-org/research/cancer-facts-and-statistics/global-cancer-facts-and-figures/global-cancer-facts-and-figures-3rd-edition.pdf. Accessed January 2019.
15. Cancer Facts & Figures 2018. American Cancer Society. Available at: https://www.cancer.org/content/dam/cancer-org/research/cancer-facts-and-statistics/annual-cancer-facts-and-figures/2018/cancer-facts-and-figures-2018.pdf. Accessed January 2019.




