Redacción Farmacosalud.com
La compañía biotecnológica Biogen ha anunciado que el Comité de Medicamentos de Uso Humano (CHMP, por sus siglas en inglés) de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) ha emitido una opinión positiva recomendando la aprobación de Nusinersen (SPINRAZA®) para el tratamiento de la Atrofia Muscular Espinal con alteraciones del cromosoma 5q. Este tipo de AME es la forma más común de esta enfermedad neuromuscular genética, llegando a representar aproximadamente el 95%[1] de todos los casos. La revisión de nusinersen se realizó bajo el procedimiento de evaluación acelerada del CHMP, un mecanismo regulatorio que tiene por objetivo proporcionar, en el menor tiempo posible, el acceso a los pacientes a los medicamentos que cubren necesidades médicas aún no satisfechas. Su aprobación en Europa convertiría a esta terapia en el primer tratamiento disponible para AME con alteraciones en la región cromosómica 5q.
La decisión positiva del CHMP se remitirá ahora a la Comisión Europea (CE), organismo encargado de conceder la autorización de comercialización a los medicamentos centralizados autorizados en la Unión Europea. Se espera poder conocer su decisión final en los próximos meses. La recomendación positiva del CHMP se basa en los resultados de dos estudios pivotales controlados, el ENDEAR[2] (AME de inicio en la infancia) y el CHERISH[3] (AME de inicio tardío), que demostraron una eficacia clínicamente significativa y un perfil de seguridad favorable de nusinersen. Este fármaco se administra mediante una inyección.
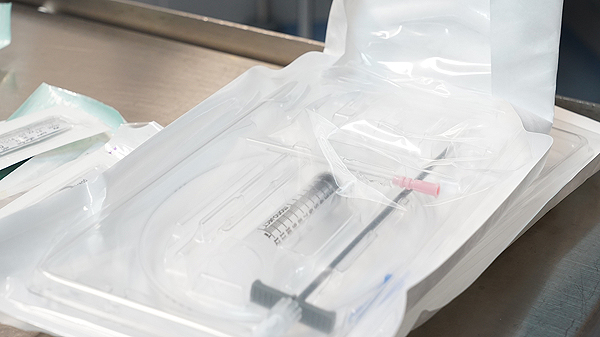
Autor/a de la imagen: E. Arandes / www.farmacosalud.com
Fuente: Gentileza del Hospital Sagrat Cor de Barcelona
▪ En el estudio ENDEAR, un porcentaje significativo de pacientes con AME de inicio en la infancia (con mayor probabilidad de desarrollar AME tipo 1) tratados con nusinersen alcanzaron una respuesta favorable en el desarrollo motor en comparación con el grupo que no fue tratado con esta terapia. Los hitos del desarrollo motor logrados en algunos pacientes tratados con nusinersen incluyeron la habilidad para mover las piernas, controlar la cabeza, rodar, sentarse y gatear. Además, se observó una reducción estadísticamente significativa en el riesgo de muerte o ventilación permanente en los pacientes tratados con nusinersen frente al grupo no tratado en el análisis final[2].
▪ El estudio CHERISH mostró una mejoría estadística y clínicamente significativa en la función motora en los pacientes con AME de inicio tardío tratados con nusinersen (con más probabilidades de desarrollar los tipos 2 o 3) en comparación con aquellos otros que no fueron tratados en el análisis temporal. Las mejoras clínicas se midieron mediante la Escala de Valoración Funcional de Hammersmith (HFMSE, por sus siglas en inglés). La HFMSE es una herramienta fiable y válida, específicamente diseñada para evaluar la función motora en niños con AME.
▪ Los datos de los estudios abiertos[4] en individuos pre-sintomáticos y sintomáticos con mayor probabilidad de desarrollar los tipos 1, 2 o 3 fueron consistentes con los resultados de los estudios pivotales[2,3] y se consideraron como apoyo de la indicación recomendada. Los resultados generales de estos estudios respaldan la eficacia y seguridad de nusinersen en pacientes con AME con alteraciones en la región cromosómica 5q.
▪ Nusinersen ha demostrado un perfil favorable de seguridad, debiendo ser administrado por profesionales sanitarios con experiencia en el procedimiento de punción lumbar, debido a las reacciones adversas asociadas al mismo tales como dolor de cabeza, dolor de espalda o vómito[4].
La AME se caracteriza por la pérdida de neuronas motoras
Biogen obtuvo los derechos mundiales para desarrollar, fabricar y comercializar nusinersen de la empresa Ionis Pharmaceuticals (NASDAQ: IONS). Biogen e Ionis llevaron a cabo un innovador programa de desarrollo clínico que ha permitido a nusinersen evolucionar de su primera dosis en seres humanos en 2011 a su primera aprobación regulatoria por parte de la Agencia Americana del Medicamento (FDA, por sus siglas en inglés) en 2016[5]. Nusinersen fue aprobado en primer lugar por la FDA el 23 de diciembre de 2016 en un plazo de tres meses tras la presentación de la solicitud de autorización. Biogen también ha presentado la solicitud de autorización a las autoridades regulatorias de Japón, Canadá, Australia y Suiza, y planea iniciar presentaciones adicionales en otros países en 2017.
Fuente: www.farmacosalud.com / IMAGEN DE ARCHIVO
Gentileza del Centro Nacional de Microbiología. Instituto de Salud Carlos III de Madrid
La AME[6-7] se caracteriza por la pérdida de neuronas motoras en la médula espinal y el tronco cerebral, provocando como resultado atrofia muscular severa progresiva y debilidad. En última instancia, las personas con el tipo más grave de AME pueden paralizarse y tienen dificultad para realizar las funciones básicas de la vida, como la respiración y la deglución. La pérdida o defecto en el gen SMN1 implica que las personas con AME no producen suficiente proteína de supervivencia de las neuronas motoras (SMN) y este hecho es crítico para el mantenimiento de las neuronas motoras. La gravedad de la AME se correlaciona con la cantidad de proteína SMN. Las personas con AME tipo 1, la forma que requiere el cuidado más intensivo, producen muy poca proteína de SMN y no logran la capacidad de sentarse sin apoyo o vivir más de dos años sin ayuda respiratoria. Las personas con AME tipo 2 y tipo 3 producen mayores cantidades de proteína SMN y presentan formas de AME menos severas pero que, igualmente, alteran y condicionan su calidad de vida.
El fármaco, un oligonucleótido antisentido (ASO)
Nusinersen es un oligonucleótido antisentido (ASO) desarrollado globalmente y diseñado para tratar la AME causada por mutaciones o delecciones en el gen SMN1. Este gen está localizado en la región cromosómica 5q y es el que conduce a la deficiencia de la proteína SMN. Nusinersen altera el empalme del pre-ARNm del SMN2 con el fin de aumentar la producción de proteína SMN de longitud completa[7]. Los ASOs son cadenas cortas sintéticas de nucleótidos, diseñados para unirse selectivamente al ARN diana y regular la expresión génica. Mediante el uso de esta tecnología, nusinersen tiene el potencial de aumentar la cantidad de proteína SMN de longitud completa en individuos con AME.
Nusinersen se administra mediante una inyección por vía intratecal, lo que permite que el tratamiento llegue directamente al líquido cefalorraquídeo (LCR) situado alrededor de la médula espinal[8], donde las neuronas motoras se degeneran en pacientes con AME debido a niveles insuficientes de proteína SMN[9]. Existe el riesgo de que se produzcan reacciones adversas como parte del procedimiento de punción lumbar (por ejemplo, dolor de cabeza, dolor de espalda o vómito). Se han observado anomalías en la coagulación y trombocitopenia, incluyendo trombocitopenia aguda grave, después de la administración de algunos oligonucleótidos antisentido, así como toxicidad renal[4].
Referencias
1. Farrar MA, Kiernan MC. The Genetics of Spinal Muscular Atrophy: Progress and Challenges. Neurotherapeutics; 2015; 12:290–302.
2. Disponible en: https://clinicaltrials.gov/ct2/show/NCT02193074?term=ENDEAR&rank=1 Última visita 24/04/2017
3. Disponible en https://clinicaltrials.gov/ct2/show/NCT02292537?term=cherish&rank=1 Última visita 24/04/2017
4. Disponible en https://clinicaltrials.gov/ct2/show/NCT02386553?term=nusinersen&rank=1 Última visita 26/04/2017
5. Biogen. SPINRAZA USPI. December 2016 https://www.accessdata.fda.gov/drugsatfda_docs/label/2016/209531lbl.pdf
6. Darras B, Markowitz J, Monani U, De Vivo D. Chapter 8 - Spinal Muscular Atrophies. In: Vivo BTD, ed. Neuromuscular Disorders of Infancy, Childhood, and Adolescence (Second Edition). San Diego: Academic Press; 2015:117-145.
7. Hua Y, Sahashi K, Hung G, Rigo F, Passini MA, Bennett CF, Krainer AR. Antisense correction of SMN2 splicing in the CNS rescues necrosis in a type III SMA mouse model. Genes Dev. 2010 Aug 1; 24(15):16344-44.
8. Evers MM, Toonen LJ, van Roon-Mom WM. Antisense oligonucleotides in therapy for neurodegenerative disorders. Adv Drug Deliv Rev. 2015;87:90-103.
9. Lunn MR, Wang CH. Spinal muscular atrophy. Lancet. 2008;371(9630):2120-2133.




