Redacción Farmacosalud.com
En el presente informe se reseñan los medicamentos ya evaluados por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), considerados de mayor interés para el profesional sanitario. Se trata de opiniones técnicas positivas de la AEMPS correspondientes al mes de octubre que son previas a la autorización y puesta en el mercado del medicamento, lo que sucederá dentro de algunos meses, informa este organismo mediante un comunicado. Una vez los nuevos fármacos se hayan autorizado, toda la información de cada uno de ellos (desde la ficha técnica y prospecto, hasta sus condiciones de prescripción, uso y disponibilidad real en el mercado) se podrá consultar en la web de la AEMPS, dentro de la sección CIMA: Centro de Información Online de Medicamentos de la AEMPS.
Baqsimi (GLUCAGÓN)
Indicación aprobada: Indicado para el tratamiento de la hipoglucemia grave en adultos, adolescentes y niños de 4 años y mayores con diabetes mellitus. Baqsimi estará disponible como polvo nasal (3 mg).
Ervebo -VACUNA PARA EBOLAVIRUS ZAIRE (RVSVΔG-ZEBOV-GP, VIVA)-
Indicación aprobada: Indicado para la inmunización activa de personas de 18 años de edad o mayores para protegerse contra la enfermedad por el virus del Ébola (EVE) causada por el ebolavirus Zaire. Ervebo estará disponible como solución para inyección. El Comité Europeo de Evaluación de Medicamentos (CHMP) ha recomendado de manera condicional la autorización de comercialización, al satisfacer una necesidad médica no cubierta, en la medida en que, el beneficio para la salud pública de su inmediata disponibilidad es superior al riesgo inherente de que todavía se requieran datos adicionales.
Evenity (ROMOSOZUMAB)
Indicación aprobada: Indicado en el tratamiento de la osteoporosis grave en mujeres posmenopáusicas con alto riesgo de fracturas. Evenity estará disponible como solución para inyección (105 mg).
Quofenix (DELAFLOXACINO)
Indicación aprobada: Indicado para el tratamiento de infecciones bacterianas agudas de piel y tejidos blandos en adultos cuando se considera inapropiado el uso de otros agentes antibacterianos que se recomiendan comúnmente para el tratamiento inicial de estas infecciones. Quofenix estará disponible como polvo para concentrado para solución para perfusión (300 mg) y en comprimidos (450 mg).
Rinvoq (UPADACITINIB)
Indicación aprobada: Indicado para el tratamiento de la artritis reumatoide activa de moderada a grave en pacientes adultos que han respondido inadecuadamente o que son intolerantes a uno o más fármacos antirreumáticos modificadores de la enfermedad (FAMEs). Rinvoq puede ser utilizado en monoterapia o en combinación con metotrexato. Rinvoq estará disponible como comprimidos de liberación prolongada (15 mg).
Spravato (ESKETAMINA)
Indicación aprobada: Spravato, en combinación con un inhibidor selectivo de la recaptación de serotonina (ISRS) o inhibidores de la recaptación de serotonina/noradrenalina (IRSN), está indicado para adultos con trastorno depresivo mayor resistente al tratamiento, que no han respondido al menos a dos tratamientos diferentes con antidepresivos en el episodio de moderado a grave depresivo actual.
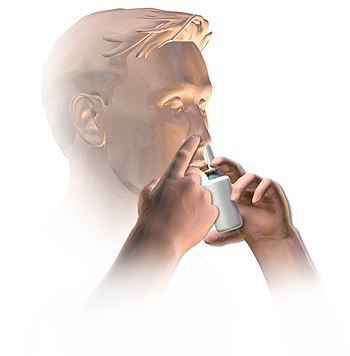
(Imagen modificada) Autor/a de la imagen original: BruceBlaus - Own work
Fuente: Wikipedia
Spravato estará disponible como solución en spray nasal (28 mg).
Biosimilares
Pegfilgrastim Mundipharma (PEGFILGRASTIM). Indicación aprobada: Indicado para la reducción de la duración de la neutropenia y de la incidencia de neutropenia febril en pacientes adultos con tumores malignos tratados con quimioterapia citotóxica (con excepción de leucemia mieloide crónica y síndromes mielodisplásicos).
Cambios de especial interés sanitario en medicamentos ya autorizados
Nuevas indicaciones con dictamen positivo para su autorización
Para las indicaciones ya autorizadas se recomienda consultar el texto completo de las mismas en las fichas técnicas disponibles en la web de la AEMPS, dentro de la sección CIMA: Centro de Información Online de Medicamentos de la AEMPS.
Darzalex (DARATUMUMAB)
Extensión de la indicación (en negrita): DARZALEX está indicado: en combinación con lenalidomida y dexametasona o con bortezomib, melfalán y prednisona para el tratamiento de pacientes adultos con mieloma múltiple de nuevo diagnóstico que no son candidatos a un trasplante autólogo de progenitores hematopoyéticos. En combinación con lenalidomida y dexametasona, o bortezomib y dexametasona, para el tratamiento de pacientes adultos con mieloma múltiple que han recibido al menos un tratamiento previo. En monoterapia para el tratamiento de pacientes adultos con mieloma múltiple en recaída y refractario al tratamiento, que hayan recibido previamente un inhibidor del proteasoma y un agente inmunomodulador y que hayan presentado progresión de la enfermedad en el último tratamiento.
Kalydeco (IVACAFTOR)
Extensión de la indicación (en negrita): Kalydeco granulado está indicado para el tratamiento de lactantes de al menos 6 meses de edad y niños con un peso de 5 kg a menos de 25 kg con fibrosis quística (FQ) y con una de las siguientes mutaciones de apertura del canal (clase III) en el gen CFTR: G551D, G1244E, G1349D, G178R, G551S, S1251N, S1255P, S549N o S549R.
Keytruda (PEMBROLIZUMAB)
Extensión de la indicación (en negrita): Keytruda en monoterapia está indicado para el tratamiento del melanoma avanzado (irresecable o metastásico) en adultos. Keytruda en monoterapia está indicado para el tratamiento adyuvante en adultos con melanoma en estadio III y con afectación de los ganglios linfáticos que hayan sido sometidos a resección completa. Keytruda en monoterapia está indicado para el tratamiento de primera línea del cáncer de pulmón no microcítico (CPNM) metastásico en adultos cuyos tumores expresen PD-L1 con una proporción de marcador tumoral (TPS, por sus siglas en inglés) ≥50% sin mutaciones tumorales positivas de EGFR o ALK. Keytruda, en combinación con pemetrexed y quimioterapia basada en platino está indicado para el tratamiento de primera línea del CPNM no escamoso metastásico en adultos cuyos tumores no tengan mutaciones tumorales positivas de EGFR o ALK.
Autor/a: DarkoStojanovic
Fuente: Pixabay (free photo)
Keytruda, en combinación con carboplatino y paclitaxel o nab-paclitaxel, está indicado para el tratamiento de primera línea del CPNM escamoso metastásico en adultos. Keytruda en monoterapia está indicado para el tratamiento del CPNM localmente avanzado o metastásico en adultos cuyos tumores expresen PD-L1 con una TPS ≥1% y que hayan recibido al menos un tratamiento de quimioterapia previo. Los pacientes con mutaciones tumorales positivas de EGFR o ALK deben haber recibido también terapia dirigida antes de recibir Keytruda.
Keytruda en monoterapia está indicado para el tratamiento de pacientes adultos con linfoma de Hodgkin clásico (LHc) en recaída o refractario, que no han respondido a un trasplante autólogo de progenitores hematopoyéticos (TAPH) y a brentuximab vedotina (BV), o que no son candidatos a trasplante y no han respondido a BV. Keytruda en monoterapia está indicado para el tratamiento del carcinoma urotelial localmente avanzado o metastásico en adultos que hayan recibido quimioterapia previa basada en platino. Keytruda en monoterapia está indicado para el tratamiento del carcinoma urotelial localmente avanzado o metastásico en adultos que no son candidatos a quimioterapia basada en cisplatino y cuyos tumores expresen PD-L1 con una puntuación positiva combinada (CPS, por sus siglas en inglés) ≥ 10.
Keytruda, como monoterapia o en combinación con platino y quimioterapia con 5-fluorouracilo (5-FU), está indicado para el tratamiento de primera línea del carcinoma de células escamosas de cabeza y cuello (CCECC) metastásico o no resecable recurrente en adultos cuyos tumores expresen PD-L1 con un CPS ≥ 1. Keytruda en monoterapia está indicado para el tratamiento del carcinoma de células escamosas de cabeza y cuello (CCECC) recurrente o metastásico en adultos cuyos tumores expresen PD-L1 con una TPS ≥ 50% y que progresen durante o después de quimioterapia basada en platino. Keytruda, en combinación con axitinib, está indicado para el tratamiento de primera línea del carcinoma de células renales avanzado (CCR) en adultos.
Toujeo (INSULINA GLARGINA)
Extensión de la indicación (en negrita): Tratamiento de diabetes mellitus en adultos, adolescentes y niños de 6 años de edad y mayores.