Redacción Farmacosalud.com
En el presente informe se reseñan los medicamentos ya evaluados por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), considerados de mayor interés para el profesional sanitario. Se trata de opiniones técnicas positivas de la AEMPS correspondientes al mes de febrero que son previas a la autorización y puesta en el mercado del medicamento, lo que sucederá dentro de algunos meses, informa este organismo mediante un comunicado. Una vez los nuevos fármacos se hayan autorizado, toda la información de cada uno de ellos (desde la ficha técnica y prospecto, hasta sus condiciones de prescripción, uso y disponibilidad real en el mercado) se podrá consultar en la web de la AEMPS, dentro de la sección CIMA: Centro de Información Online de Medicamentos de la AEMPS.
Dectova (ZANAMIVIR)
Indicación aprobada: Dectova está indicado en adultos y niños (con edad ≥ 6 meses) para el tratamiento de gripe A o B complicada y potencialmente mortal cuando: El virus de la gripe identificado en el paciente es resistente, o se sospecha que lo sea, a medicamentos para el tratamiento de la gripe distintos de zanamivir y/o, otros medicamentos antivirales, para el tratamiento de la gripe, incluido zanamivir inhalado, no son adecuados para el paciente. Dectova estará disponible como solución para infusión (10 mg/mL).
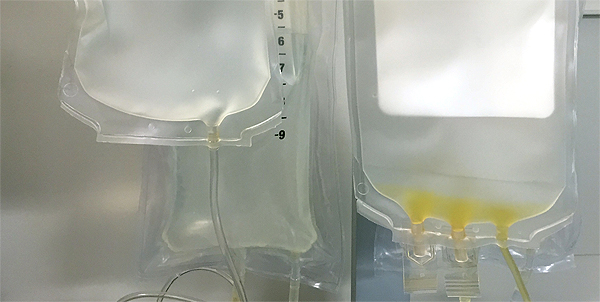
Material para el proceso de infusión intravenosa
(imagen modificada) Autor/a de la imagen original: NIAID
Fuente. Flickr / Creative Commons
Lorviqua (LORLATINIB)
Indicación aprobada: Lorlatinib, en monoterapia está indicado para el tratamiento de pacientes adultos con cáncer de pulmón no microcítico (CPNM) avanzado, positivo para quinasa de linfoma anaplásico (ALK), que han progresado tras tratamiento con: alectinib o ceritinib como primer inhibidor de tirosin-quinasa (TKI) ALK; o crizotinib y al menos otro ALK -TKI. Lorviqua estará disponible como comprimidos recubiertos con película (25 y 100 mg).
Ondexxya (ANDEXANET ALFA)
Indicación aprobada: Ondexxya está indicado para pacientes adultos tratados con un inhibidor directo del factor Xa (apixaban o rivaroxaban) cuando es necesario revertir la anticoagulación debido a hemorragias incontroladas o potencialmente mortales. Ondexxya estará disponible como 200 mg de polvo para solución para infusión.
Palynziq (PEGVALIASE)
Indicación aprobada: Palynziq está indicado para el tratamiento de pacientes de 16 años de edad y mayores con fenilcetonuria con un control inadecuado de los niveles de fenilalanina en sangre (niveles de fenilalanina mayores de 600 micromol/L) a pesar de haber sido tratados con las alternativas disponibles. Palynziq estará disponible como solución para inyección (2,5, 10 y 20 mg).
Skyrizi (RISANKIZUMAB)
Indicación aprobada: Skyrizi está indicado para el tratamiento de la psoriasis en placas de moderada a grave en adultos que son candidatos a tratamientos sistémicos. Skyrizi estará disponible como solución para inyección (75 mg).
Waylivra (VOLANESORSEN)
Indicación aprobada: Waylivra está indicado como complemento a la dieta en pacientes adultos con síndrome de quilomicronemia familiar confirmado y con riesgo elevado de pancreatitis, que tienen una respuesta inadecuada a la dieta y tratamientos hipolipemiantes. Waylivra estará disponible como solución para inyección (285 mg).
Zynquista (SOTAGLIFLOZIN)
Indicación aprobada: Zynquista está indicado como complemento a la insulina en adultos con diabetes mellitus tipo 1 con un IMC ≥ 27 kg/m2, para mejorar el control glucémico cuando la insulina en monoterapia no proporciona un control glucémico adecuado a pesar de una dosis de insulina óptima. Zynquista estará disponible como comprimidos recubiertos con película (200 mg).
Cambios de especial interés sanitario en medicamentos ya autorizados
Nuevas indicaciones con dictamen positivo para su autorización
Para las indicaciones ya autorizadas se recomienda consultar el texto completo de las mismas en las fichas técnicas disponibles en la web de la AEMPS, dentro de la sección CIMA: Centro de Información Online de Medicamentos de la AEMPS.
Dupixent (DUPILUMAB)
Extensión de la indicación (en negrita): Dermatitis atópica. Dupixent está indicado para el tratamiento de la dermatitis atópica de moderada a grave en pacientes adultos que son candidatos a tratamiento sistémico. Asma. Dupixent está indicado como tratamiento de mantenimiento adicional en adultos y adolescentes de 12 años de edad y mayores con asma grave con inflamación tipo 2 caracterizada por un aumento de los eosinófilos y/o elevación de la fracción de óxido nítrico exhalado, que no están adecuadamente controlados a pesar de la administración de corticosteroides inhalados en dosis altas más otro medicamento para el tratamiento de mantenimiento.
Lynparza (OLAPARIB)

Autor/a de la imagen: Enric Arandes
Fuente: E. Arandes / www.farmacosalud.com
Extensión de la indicación (en negrita): Cáncer de ovario. Lynparza está indicado como monoterapia para el tratamiento de mantenimiento de pacientes adultas con cáncer de ovario epitelial de alto grado, trompa de Falopio, o peritoneal primario, en recaída, sensible a platino, que están en respuesta (completa o parcial) a quimioterapia basada en platino. Cáncer de mama. Lynparza está indicado como monoterapia para el tratamiento de pacientes adultos con mutaciones BRCA1/2 germinales, con cáncer de mama localmente avanzado o metastásico HER2 negativo. Los pacientes deben haber sido previamente tratados con una antraciclina y un taxano en ámbito neoadyuvante o metastásico, a no ser que los pacientes no sean candidatos a estos tratamientos. Los pacientes con cáncer de mama con receptor hormonal positivo deben haber progresado durante o después del tratamiento endocrino previo, o no considerarse candidatos al tratamiento endocrino.
Riarify / Trydonis (BECLAMETASONA DIPROPIONATO / FORMOTEROL FUMARATO DEHIDRATO / GLICOPIRRONIO)
Extensión de la indicación (en negrita): Tratamiento de mantenimiento en los pacientes adultos con enfermedad pulmonar obstructiva crónica (EPOC) moderada a grave que no están adecuadamente controlados con una combinación de un corticoesteroide inhalado y un agonista beta2 de acción prolongada o una combinación de un agonista beta2 de acción prolongada y un antagonista muscarínico de acción prolongada.
Viread (TENOFOVIR DISOPROXILO) 123 mg
Extensión de la indicación (en negrita): Infección por VIH-1. Viread 123 mg comprimidos recubiertos con película está indicado en combinación con otros fármacos antirretrovirales para el tratamiento de pacientes pediátricos infectados por el VIH-1, con resistencia a los ITIAN o toxicidades que impidan el uso de fármacos de primera línea, de 6 a < 12 años, que pesen entre 17 kg y menos de 22 kg. Infección por hepatitis B. Viread 123 mg comprimidos recubiertos con película está indicado para el tratamiento de la hepatitis B crónica en pacientes pediátricos, de 6 a < 12 años, que pesen entre 17 kg y menos de 22 kg con: enfermedad hepática compensada y evidencia de enfermedad inmune activa, es decir, replicación viral activa y niveles séricos de ALT persistentemente elevados o evidencia histológica de inflamación de moderada a grave y/o fibrosis.
Viread (TENOFOVIR DISOPROXILO) 163 mg
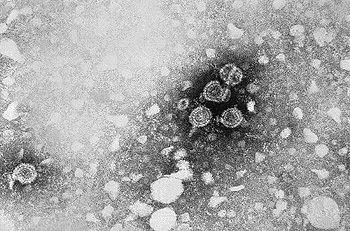
Micrografía que muestra viriones de hepatitis B
Autor/a de la imagen: CDC/Dr. Erskine Palmer (PHIL #270), 1981.
Fuente: Wikipedia
Extensión de la indicación (en negrita): Infección por VIH-1. Viread 163 mg comprimidos recubiertos con película está indicado en combinación con otros fármacos antirretrovirales para el tratamiento de pacientes pediátricos infectados por el VIH-1, con resistencia a los ITIAN o toxicidades que impidan el uso de fármacos de primera línea, de 6 a < 12 años, que pesen entre 22 kg y menos de 28 kg. La elección de Viread como tratamiento antirretroviral en pacientes con infección por VIH-1 pretratados debe basarse en la prueba de resistencia viral del paciente y/o el historial de tratamiento de los pacientes. Infección por hepatitis B. Viread 163 mg comprimidos recubiertos con película está indicado para el tratamiento de la hepatitis B crónica en pacientes pediátricos, de 6 a < 12 años, que pesen entre 22 kg y menos de 28 kg, con: enfermedad hepática compensada y evidencia de enfermedad inmune activa, es decir, replicación viral activa y niveles séricos de ALT persistentemente elevados o evidencia histológica de inflamación de moderada a grave y/o fibrosis.
Viread (TENOFOVIR DISOPROXILO) 204 mg
Extensión de la indicación (en negrita): Infección por VIH-1. Viread 204 mg comprimidos recubiertos con película está indicado en combinación con otros fármacos antirretrovirales para el tratamiento de pacientes pediátricos infectados por el VIH-1, con resistencia a los ITIAN o toxicidades que impidan el uso de fármacos de primera línea, de 6 a < 12 años, que pesen entre 28 kg y menos de 35 kg. Infección por hepatitis B. Viread 204 mg comprimidos recubiertos con película está indicado para el tratamiento de la hepatitis B crónica en pacientes pediátricos, de 6 a < 12 años, que pesen entre 28 kg y menos de 35 kg, con: enfermedad hepática compensada y evidencia de enfermedad inmune activa, es decir, replicación viral activa y niveles séricos de ALT persistentemente elevados o evidencia histológica de inflamación de moderada a grave y/o fibrosis.
Viread (TENOFOVIR DISOPROXILO) 33 mg/g en gránulos
Extensión de la indicación (en negrita): Infección por VIH-1. Viread 33 mg/g gránulos está indicado en combinación con otros fármacos antirretrovirales para el tratamiento de pacientes pediátricos infectados por el VIH-1, con resistencia a los ITIAN o toxicidades que impidan el uso de fármacos de primera línea, de 2 a < 6 años, y mayores de 6 años para quienes no sea adecuada una forma farmacéutica sólida. Viread 33 mg/g gránulos está indicado también en combinación con otros fármacos antirretrovirales para el tratamiento de adultos infectados por el VIH-1 para quienes no sea adecuada una forma farmacéutica sólida. Infección por hepatitis B. Viread 33 mg/g gránulos está indicado para el tratamiento de la hepatitis B crónica en adultos para quienes no sea adecuada una forma farmacéutica sólida con: enfermedad hepática compensada, con evidencia de replicación viral activa, con niveles plasmáticos de alanina aminotransferasa (ALT) elevados de forma continuada y evidencia histológica de inflamación activa y/o fibrosis. evidencia de virus de la hepatitis B con resistencia a lamivudina. Enfermedad hepática descompensada.
Viread 33 mg/g gránulos está indicado también para el tratamiento de la hepatitis B crónica en pacientes pediátricos de 2 a < 18 años de edad para quienes no sea adecuada una forma farmacéutica sólida con: enfermedad hepática compensada y evidencia de enfermedad inmune activa, es decir, replicación viral activa, niveles séricos de ALT persistentemente elevados y evidencia histológica de inflamación activa y/o fibrosis.