Redacción Farmacosalud.com
Hemlibra® (emicizumab), la primera novedad terapéutica en 20 años para la hemofilia A con inhibidores, llega a España como tratamiento de la hemofilia A con inhibidores del factor VIII, informa la compañía Roche. Según el Dr. Víctor Jiménez Yuste, jefe del Servicio de Hematología del Hospital Universitario La Paz (Madrid), la gran eficacia que ha demostrado el nuevo fármaco incluso “ha conseguido alcanzar el sangrado cero, algo que no se había logrado con las terapias actuales”. Si bien cualquiera de estos pacientes es subsidiario de ser tratado con emicizumab en pos del sangrado cero, este objetivo “es más factible y más fácil de lograr en niños o adolescentes que previamente no presenten daño articular establecido”, precisa a www.farmacosalud.com el Dr. Ramiro Núñez, jefe de la sección de Trombosis y Hemostasia de la U.G.C de Hematología del Hospital Universitario Virgen del Rocío (Sevilla).
La hemofilia A es la forma más grave de la enfermedad y representa aproximadamente el 80% del total de casos de esta patología, que afecta en torno a 3.000 personas en España. El Ministerio de Sanidad, Consumo y Bienestar Social ha aprobado la financiación de Hemlibra como tratamiento para este tipo de hemofilia en los pacientes que han desarrollado inhibidores a las terapias de reemplazo del factor VIII, aproximadamente un tercio del total. Las personas con hemofilia A que desarrollan inhibidores se exponen a un alto riesgo de hemorragias potencialmente mortales y de sangrados de repetición que, a largo plazo, pueden causar daños en las articulaciones, lo que a su vez puede ocasionar problemas de movilidad.
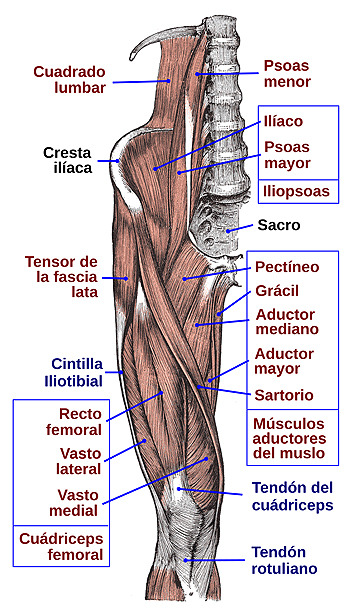
Psoas ilíaco (músculo iliopsoas, o psoas-ilíaco o psoasilíaco) etiquetado arriba a la izquierda
Músculos de la cara anterior del muslo y pelvis, adaptación de los dibujos de la Anatomía de Gray
Autor/a de la imagen: Jmarchn - Trabajo propio, basado en: Gray430.png
Fuente: Wikipedia
Los peligros de la hemorragia del músculo psoasilíaco
Una persona que sufre hemofilia A con inhibidores puede sangrar espontáneamente, no hace falta que se lesione, caiga o se hiera. Lógicamente, los sangrados espontáneos son más difíciles de controlar. Además, los episodios hemorrágicos que padecen esos sujetos pueden ser visibles o bien pueden manifestarse como hemorragias internas. “Lo más frecuente es que sean hemorragias visibles, fundamentalmente en las articulaciones, que se inflaman causando una gran impotencia y dolor articular. Pero también pueden ser internas; por ejemplo, una muy habitual en estos pacientes es la hemorragia del músculo psoasilíaco”, explica Núñez. Se trata de un músculo que está situado en el abdomen y que tiene una gran funcionalidad en la elevación de las piernas. Los sangrados en el órgano psoasilíaco, al no ser visibles, pueden ser potencialmente peligrosos, e incluso, muy excepcionalmente, pueden llegar a causar la muerte.
La financiación de Hemlibra en esta indicación se produce después de que la Comisión Europea (CE) aprobase el pasado año esta terapia como tratamiento profiláctico de rutina para prevenir episodios de sangrado en pacientes con hemofilia A e inhibidores del factor VIII en todos los grupos de edad. Según la Dra. Beatriz Pérez, directora médica de Roche Farma España, “Hemlibra es fruto de una importante apuesta por la innovación y una muestra del compromiso que Roche ha adquirido con la comunidad de la hemofilia. Estamos muy orgullosos de poner a disposición de las personas con hemofilia A e inhibidores esta nueva opción. No debemos olvidar que el desarrollo de inhibidores incrementa en un 70% el riesgo de muerte respecto al no desarrollo de los mismos, y que, hasta ahora, las personas en esta situación contaban con opciones terapéuticas limitadas”, recuerda.
Sobre el programa de desarrollo clínico HAVEN
La aprobación de esta indicación se ha basado en los datos de los ensayos HAVEN 1 y HAVEN 2, en los que se ha demostrado una eficacia superior de Hemlibra en comparación con el tratamiento previo con agentes de by-pass en profilaxis. Concretamente, según los resultados del ensayo HAVEN 1 en adultos y adolescentes, la profilaxis con Hemlibra mostró una reducción estadísticamente significativa en las hemorragias tratadas del 87% (ratios de riesgo (RR)=0,13, p<0,0001) en comparación con los que no recibieron profilaxis. Por otra parte, los resultados del estudio HAVEN 2 en niños menores de 12 años con hemofilia A e inhibidores mostraron una reducción del riesgo de sangrados tratados del 99% (IC 95%: 97.7-99.4) en niños que recibieron profilaxis con Hemlibra comparado con tratamiento anterior con agentes de by-pass en una comparación intra-individual con agentes de by-pass en profilaxis.
El programa de desarrollo clínico HAVEN para pacientes con hemofilia A con inhibidores ha contado con la participación de 5 hospitales españoles. En palabras de la Dra. Pérez, “España ha sido el país, después de Estados Unidos, en el que más pacientes han participado en los ensayos con esta terapia, aportando en algunos de ellos el primer paciente a nivel global o europeo, lo que ha permitido que muchas personas con hemofilia en España hayan podido beneficiarse del tratamiento antes de su aprobación definitiva”.
A juicio del Dr. Jiménez Yuste, emicizumab va a suponer un cambio radical en la cotidianeidad de estos pacientes hemofílicos, “ya que por fin disponen de una profilaxis de los episodios hemorrágicos realmente efectiva”. “Su aprobación, sin duda -agrega-, supone todo un logro que no solo modificará el abordaje de la enfermedad, sino también la vida de los pacientes”. En este sentido, el Dr. Núñez resalta a través de un comunicado que emicizumab “no sólo ofrece una profilaxis similar o superior a los tratamientos ya existentes, sino que además cuenta con la ventaja añadida de la administración subcutánea, lo que sin duda supone un avance cualitativo en la calidad de vida de los pacientes al reducir la carga del tratamiento”.
Autor/a: qimono
Fuente: Pixabay / Creative Commons
Así pues, la aplicación subcutánea permite que no haya que ‘encontrar la vena’ durante el proceso de inyección, con lo que, directamente, se hace un pellizquito en la piel y se procede a pinchar con la aguja. Para la hemofilia A, en general, los tratamientos hasta ahora disponibles se basan en la vía intravenosa. Dado que el tratamiento para esas personas es profiláctico -se pretende evitar que se produzcan episodios hemorrágicos-, se procede a aplicar dicha profilaxis 2 o 3 veces por semana, por lo que “es fácil de entender que la administración de un fármaco por vía subcutánea una vez a la semana -como es el caso de emicizumab- suponga un gran impacto en la calidad de vida de los afectados”, remarca Núñez. El nuevo medicamento, además, se puede administrar en casa, lo que “otorga a los pacientes una autonomía digna de mención”, destaca.
La opción intravenosa presenta el problema de la canalización de la vía
Tradicionalmente, los pacientes con hemofilia A e inhibidores se han venido tratando con agentes de by-pass cada 24 o 48 horas en profilaxis, y a demanda cuando se producen hemorragias. Los agentes by-pass son fármacos que se inyectan de forma intravenosa, infundiéndose aproximadamente por espacio de un minuto y medio o 2 minutos. Pueden administrarse hospitalariamente pero también de forma domiciliaria. El problema de la aplicación intravenosa es que exige la canalización de una vía venosa, aunque sea momentáneamente, para administrar el factor. “Es por ello que la administración subcutánea representa un cambio muy radical… de hecho, la opción subcutánea es una de las cualidades más valoradas por los pacientes, ya que esa vía evita la dificultad que supone el tener que canalizar cada vez que hay que someterse al tratamiento”, apunta el Dr. Núñez.
Canalizar una vía es más complicado cuanto más corta es la edad del paciente. De ahí que, en caso de que los pacientes estén en franja pediátrica, en ocasiones resulte necesario canalizar dispositivos permanentes -una especie de accesos venosos subcutáneos que requieren una pequeña intervención quirúrgica- con el fin de facilitar la administración del agente terapéutico. “Estos dispositivos no están exentos de complicaciones”, advierte el jefe de la sección de Trombosis y Hemostasia de la U.G.C de Hematología del Hospital Universitario Virgen del Rocío, quien a renglón seguido recuerda que la aplicación subcutánea está libre de todos esos contratiempos.

(de izq. a dcha): Drs. Víctor Jiménez Yuste, Beatriz Pérez y Ramiro Núñez
Fuente: Roche Farma / Planner Media
El principal efecto secundario que presenta emicizumab es eritema en el punto de la inyección, evento absolutamente pasajero que en ningún momento ha dado lugar a algún caso de abandono de la terapia. “Bien es verdad que hubo un subgrupo de pacientes que, en HAVEN 1, desarrollaron una complicación denominada microangiopatía trombótica, pero se descubrió que estaba relacionada con la asociación del fármaco a la administración de un agente by-pass en unas dosis superiores a las permitidas. Cuando eso se averiguó, se pusieron las advertencias necesarias, y a partir de ese momento ya no se produjo ningún evento adverso en ese sentido”, detalla Núñez. Emicizumab se puede utilizar en todos los grupos de edad y no presenta ninguna contraindicación, pudiendo utilizarse en pacientes con insuficiencia renal, con insuficiencia hepática o con infección por VIH, indica el galeno.
La segunda indicación, aprobada por la CE
Por otro lado, la Comisión Europea aprobó el pasado mes de marzo la indicación de Hemlibra en pacientes sin inhibidores, ámbito en el que el fármaco ha logrado reducir significativamente las hemorragias tratadas en comparación con la profilaxis previa con factor VIII en una comparación prospectiva intra-paciente. Esta indicación está pendiente de la obtención de precio y reembolso en España.
Hemlibra es un anticuerpo monoclonal biespecífico diseñado para posibilitar la asociación de los factores IXa y X, proteínas necesarias para la activación de la cascada natural de la coagulación, y restablecer el proceso de la coagulación sanguínea en pacientes con hemofilia A. Hemlibra es un tratamiento profiláctico (preventivo) que se administra por inyección bajo la piel (por vía subcutánea) de una solución lista para usar una vez por semana.
La hemofilia A es un grave trastorno genético que se produce cuando la sangre no coagula adecuadamente, causando hemorragias incontroladas y, con frecuencia, espontáneas. Afecta a cerca de 320.000 personas en todo el mundo y aproximadamente el 50-60% sufre una forma severa de hemofilia. Los afectados no tienen suficiente cantidad de la proteína de coagulación llamada factor VIII. En una persona sana, cuando ocurre una hemorragia, el factor VIII se encarga de reunir los factores de coagulación IXa y X, que es un paso clave en la formación de un coágulo de sangre para ayudar a detener la hemorragia. Dependiendo de la gravedad de su trastorno, las personas con hemofilia A pueden sangrar con frecuencia, especialmente en sus articulaciones o músculos. Estas hemorragias pueden representar un problema de salud importante, ya que a menudo causan dolor y pueden provocar inflamación crónica, deformidad, movilidad reducida y daño articular a largo plazo. Una complicación grave del tratamiento es el desarrollo de inhibidores del factor VIII a las terapias de reemplazo. Los inhibidores son anticuerpos desarrollados por el sistema inmune del cuerpo que se unen y bloquean la eficacia del factor VIII de la terapia de reemplazo, haciendo muy difícil o, incluso, imposible, obtener un nivel suficiente de la proteína factor VIII para controlar la hemorragia.




