Redacción Farmacosalud.com
La compañía MSD ha anunciado que el Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea del Medicamento (EMA) ha emitido una opinión positiva que recomienda la aprobación de KEYTRUDA® (pembrolizumab), el tratamiento anti-PD-1 de MSD, en combinación con quimioterapia con pemetrexed (ALIMTA®, de Lilly) y platino (cisplatino o carboplatino) para el tratamiento en primera línea del cáncer de pulmón no microcítico (CPNM) no escamoso metastásico en adultos cuyos tumores no tengan aberraciones tumorales genómicas en EGFR o ALK, independientemente de la expresión de PD-L1.
Si se aprueba, esto supondría la primera aprobación en Europa de un tratamiento anti-PD-1 en combinación con quimioterapia y se basa en datos de supervivencia global (SG) y supervivencia libre de progresión (SLP) del ensayo fase 3 KEYNOTE-189.
Fuente: Archivo
Opinión positiva también para el tratamiento del cáncer de cabeza y cuello
El CHMP emitió también una opinión positiva que recomienda la aprobación de pembrolizumab en monoterapia para el tratamiento del carcinoma de células escamosas de cabeza y cuello (CCECC) recidivante o metastásico en adultos cuyos tumores expresan PD-L1 con una puntuación de proporción tumoral (TPS) ≥50% y que tuvieron progresión durante o después de la exposición a quimioterapia basada en platino, de acuerdo con los datos del ensayo fase 3 KEYNOTE-040.
Estas dos recomendaciones serán revisadas ahora por la Comisión Europea para la autorización de comercialización en la Unión Europea (UE). Se espera una decisión final sobre ambas recomendaciones en el tercer trimestre de 2018.
Acerca de los cánceres de pulmón y de cabeza y cuello en Europa
El cáncer de pulmón, que se forma en los tejidos de los pulmones, habitualmente en las células que tapizan las vías aéreas, es la principal causa de muerte por cáncer en Europa y en todo el mundo. En 2012, hubo casi 354.000 muertes por tumor pulmonar en Europa. Los dos tipos principales de cáncer de pulmón son el no microcítico y el microcítico. El CPNM es el tipo más frecuente de cáncer de pulmón y representa alrededor del 85 por ciento de todos los casos, la mayoría de los cuales son de tipo no escamoso.
El cáncer de cabeza y cuello incluye varios tumores diferentes que se desarrollan en o alrededor de la garganta, la laringe, la nariz, los senos paranasales y la boca. La mayoría de los cánceres de cabeza y cuello son carcinomas de células escamosas que comienzan en las células escamosas planas que constituyen la fina capa de superficie de las estructuras de la cabeza y el cuello. Los principales factores de riesgo modificables del cáncer de cabeza y cuello incluyen el tabaco y el consumo importante de alcohol. Otros factores de riesgo incluyen la infección con determinados tipos de virus del papiloma humano (VPH). En Europa, hubo aproximadamente 140.000 nuevos casos de cáncer de cabeza y cuello en 2012 y alrededor de 63.000 personas fallecieron por esta enfermedad.

Fuente: www.farmacosalud.com / ARCHIVO
Gentileza del Centro Nacional de Microbiología. Instituto de Salud Carlos III de Madrid
Pembrolizumab, aprobado para varias indicaciones
Pembrolizumab es un tratamiento anti-PD-1 que actúa aumentando la capacidad del sistema inmunitario del cuerpo para ayudar a detectar y combatir a las células tumorales. Pembrolizumab es un anticuerpo monoclonal humanizado que bloquea la interacción entre PD-1 y sus ligandos, PD-L1 y PD-L2, activando así los linfocitos T, lo que puede afectar tanto a las células tumorales como a las células sanas. En España, pembrolizumab está financiado en el sistema público de salud en las siguientes indicaciones: en monoterapia, para el tratamiento de melanoma avanzado (irresecable o metastásico) en adultos y para el tratamiento de primera línea del cáncer de pulmón no microcítico (CPNM) metastásico en adultos cuyos tumores expresen PD-L1 con una proporción de marcador tumoral (TPS, por sus siglas en inglés) ≥50% sin mutaciones tumorales positivas de EGFR o ALK. También en monoterapia para la indicación en cáncer de pulmón no microcítico (CPNM) localmente avanzado o metastásico en adultos cuyos tumores expresen PD-L1 con una TPS ≥1% y que hayan recibido al menos un tratamiento de quimioterapia previo. Los pacientes con mutaciones de EGFR o de ALK también deben haber recibido terapia dirigida para estas alteraciones antes de recibir pembrolizumab.
Además, junto con estas indicaciones, pembrolizumab está aprobado por la Agencia Europea del Medicamento (EMA) en monoterapia para el tratamiento del carcinoma urotelial localmente avanzado o metastásico en adultos que no son candidatos a quimioterapia basada en cisplatino y cuyos tumores expresen PD-L1 con una puntuación positiva combinada (CPS; por sus siglas en inglés) ≥ 10 y en el tratamiento del carcinoma urotelial localmente avanzado o metastásico en adultos que hayan recibido quimioterapia previa basada en platino. Asimismo, está indicado en monoterapia para el tratamiento de pacientes adultos con linfoma de Hodgkin clásico (LHc) en recaída o refractario, que no han respondido a un trasplante autólogo de progenitores hematopoyéticos (TAPH) y a brentuximab vedotina (BV), o que no son candidatos a trasplante y no han respondido a BV.
Biopsia selectiva del ganglio centinela en tumores orales
Por otro lado, especialistas en Medicina Nuclear del Hospital Universitario Virgen del Rocío (Sevilla) apuestan por la biopsia selectiva del ganglio centinela para diagnosticar los tumores de la cavidad oral. Se trata de una técnica menos agresiva -se considera mínimamente invasiva- que genera menos efectos secundarios y de la que ya se han beneficiado 33 pacientes.
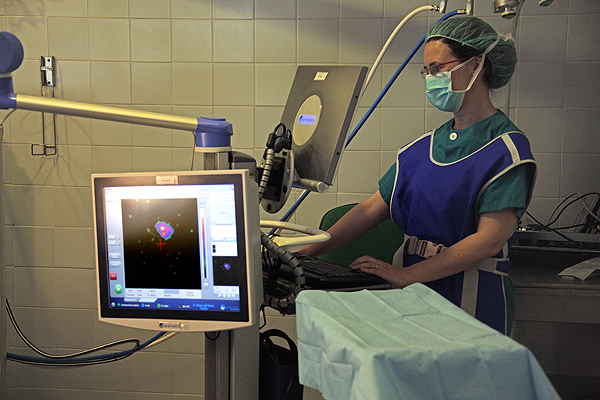
Biopsia selectiva del ganglio centinela en el ámbito del cáncer de cabeza y cuello
Fuente: Hospital Universitario Virgen del Rocío
Los profesionales de dicho centro hospitalario incluyeron hace 18 meses la biopsia selectiva del ganglio centinela, ya que es mucho menos agresiva y causa una menor morbilidad que la cirugía que con el mismo fin se venía realizando hasta ahora en estos pacientes, y que consistía en una linfadenectomia cervical (extirpar todo el sistema linfático cervical ante del riesgo de que el cáncer se extendiera a esta zona). Esta opción supone un mayor riesgo de complicaciones para el paciente al tiempo que requiere más días de ingreso hasta que recibe el alta médica.
La biopsia selectiva del ganglio centinela es una técnica que los profesionales usan de manera habitual en otros tipos de tumores, principalmente, en carcinomas mamarios y melanomas cutáneos. Se trata de un procedimiento en el que se identifica, se extirpa y se examina el ganglio linfático centinela para determinar si hay células cancerosas presentes. Un resultado negativo de dicha biopsia sugiere, por tanto, que el cáncer no ha adquirido la capacidad para diseminarse a los ganglios linfáticos cercanos o a otros órganos, por lo que se encontraría en las primeras fases de la enfermedad. Un resultado positivo, en cambio, indica que el cáncer está presente en el ganglio linfático centinela y que podría encontrarse en otros ganglios linfáticos cercanos (llamados ganglios linfáticos regionales) y, posiblemente, en otros órganos.
La información que ofrece esta prueba es, por tanto, de vital importancia para que el médico pueda determinar la extensión de la enfermedad en el cuerpo y, en función de esto, formular un plan específico de tratamiento para el paciente.




